2022年4月12日,基礎醫(yī)學院程金科教授實驗室在Cell Reports發(fā)表了題為“SENP1-Sirt3 signaling promotes α-ketoglutarate production during M2 macrophage polarization” 的研究論文,報道了SENP1-Sirt3信號軸通過調控谷氨酰胺代謝促進α酮戊二酸產生和巨噬細胞M2型極化的新機制。

巨噬細胞是機體固有免疫系統(tǒng)重要成員之一,參與病原體識別和清除,抗原遞呈和T細胞活化,啟動組織損傷修復以及調控代謝和腫瘤等疾病的微環(huán)境穩(wěn)態(tài)。巨噬細胞在不同的信號激活后形成不同的活化狀態(tài),典型的有促進炎癥反應的M1型和抑制炎癥反應的M2型。M1型巨噬細胞主要通過產生活性氧和活性氮以及諸多促炎因子,清除病原體、凋亡/壞死細胞和腫瘤細胞,是經典的巨噬細胞活化形式;而M2型巨噬細胞由于能夠抑制炎癥和免疫反應,在組織損傷修復和抗腫瘤免疫調控等方面有重要作用,近年來倍數(shù)關注。對于調控巨噬細胞M2型極化的信號通路有許多研究,但由于其復雜性,到目前依然有許多調控分子與作用機制未解。
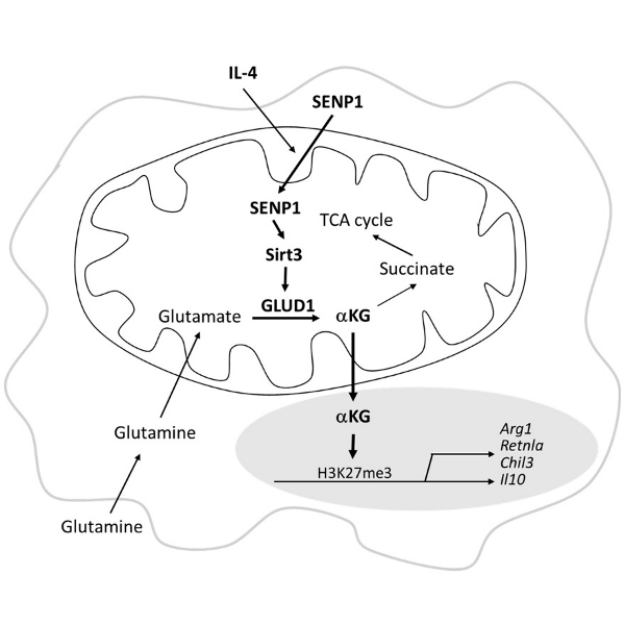
程金科教授實驗室于2019年報道了SENP1-Sirt3軸在細胞線粒體代謝應激反應中的關鍵調控作用,是細胞代謝可塑性和細胞穩(wěn)態(tài)維持的重要信號通路(Molecular Cell, 2019)。SENP1-Sirt3軸通過調控脂肪酸氧化磷酸化代謝促進記憶性T細胞形成和活化,在抗腫瘤免疫中有重要作用( Nature Communication, 2021)。在這些研究的基礎上,博士研究生周煒等進一步探討了這一通路在巨噬細胞活化過程中的作用。他們發(fā)現(xiàn)SENP1-Sirt3 信號軸活化特異性地促進IL-4誘導的巨噬細胞M2型活化。通過代謝組學和基因組學的分析,發(fā)現(xiàn)這一通路調控了谷氨酰胺分解代謝途徑中催化谷氨酸轉化為α酮戊二酸的谷氨酸脫氫酶(GLUD1)的活性,促進了α酮戊二酸的產生。α酮戊二酸是一個關鍵的表觀遺傳調控因子,能夠促進巨噬細胞M2型極化。因此,這一研究發(fā)現(xiàn)了SENP1-Sirt3軸對谷氨酰胺代謝和α酮戊二酸產生的新調控機制和這一機制對巨噬細胞M2型極化的調控作用。 這一發(fā)現(xiàn)可能為探討腫瘤代謝微環(huán)境如何影響抗腫瘤免疫提供新的思路和干預途徑。
