2021年1月11日,上海交通大學醫(yī)學院上海市免疫學研究所鄒強團隊聯(lián)合鄧劉福團隊,、上海交通大學醫(yī)學院附屬瑞金醫(yī)院王正廷副主任醫(yī)師團隊在國際著名期刊Molecular Cell在線發(fā)表了題為“SENP3 senses oxidative stress to facilitate STING-dependent dendritic cell antitumor function”的研究論文,。該研究發(fā)現(xiàn)腫瘤微環(huán)境中的活性氧增強樹突狀細胞中STING信號激活,從而促進樹突狀細胞介導的抗腫瘤免疫反應,。本研究揭示了活性氧在腫瘤微環(huán)境中促進樹突狀細胞抗腫瘤免疫的作用機理,,為開發(fā)基于干預活性氧治療腫瘤的免疫治療策略提供新的思路。

活性氧(ROS)不僅是需氧生物細胞的代謝副產物,,而且還是細胞內重要的信號分子,。ROS參與腫瘤免疫應答與耐受,其中的機制亟待深入研究,。樹突狀細胞(DC)作為專職的抗原遞呈細胞,,在腫瘤免疫應答中發(fā)揮關鍵作用。盡管已有的研究發(fā)現(xiàn)低濃度ROS對DC激活有促進作用,,高濃度ROS對DC功能有抑制作用,,但是腫瘤微環(huán)境中的DC如何感應ROS來發(fā)揮抗腫瘤功能依然不清楚。
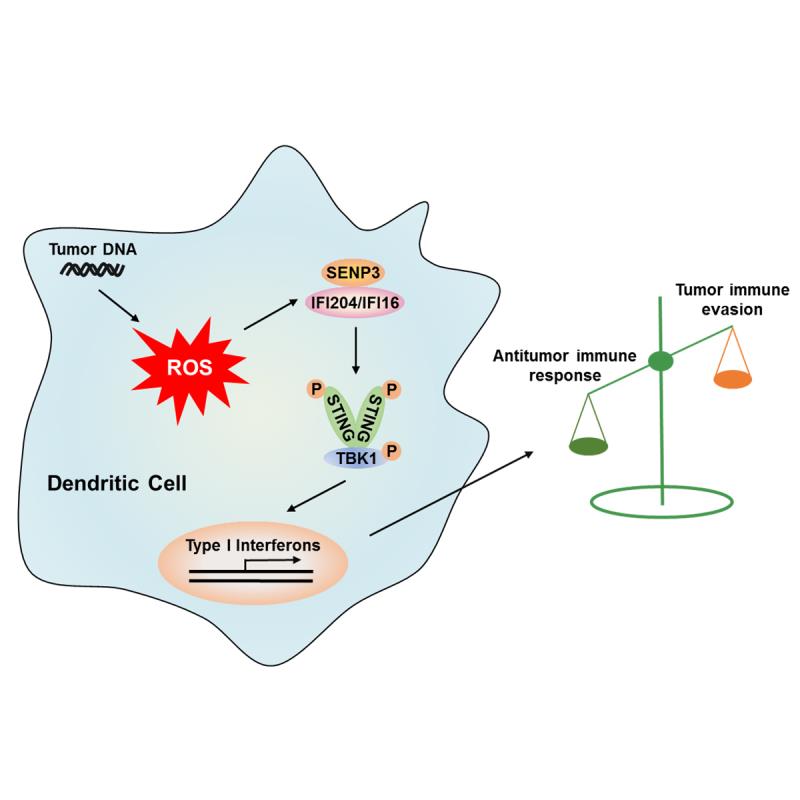
圍繞這一重要科學問題,,鄒強,、王正廷、鄧劉福團隊通力合作,,以結直腸癌為研究模型,,從ROS感應蛋白SENP3入手,發(fā)現(xiàn)結直腸癌患者腫瘤組織中的DC表達大量SENP3,;應用小鼠結直腸癌模型和臨床結直腸癌樣本,,證明腫瘤微環(huán)境中DC通過SENP3感應ROS并增強STING信號激活,,從而促進DC抗腫瘤功能;進一步的機制研究顯示:DC中的ROS介導SENP3蛋白累積,,促進DNA感應蛋白IFI16(人)或IFI204(鼠)的去類泛素化修飾,,從而增強胞質DNA誘導的STING信號激活,。本項研究闡述了代謝副產物ROS在腫瘤微環(huán)境中促進STING介導的DC抗腫瘤功能機制,,為開發(fā)基于干預活性氧治療腫瘤的免疫治療策略提供新的思路。
上海交通大學醫(yī)學院激勵計劃博士后,、上海市免疫學研究所余?博士后胡志林博士和高級實驗師滕曉鹿博士是本論文的共同第一作者,,上海交通大學醫(yī)學院上海市免疫學研究所鄒強研究員、鄧劉福研究員,、上海交通大學醫(yī)學院附屬瑞金醫(yī)院消化科王正廷副主任醫(yī)師為共同通訊作者,。該研究得到了上海交通大學基礎醫(yī)學院易靜教授和上海交通大學醫(yī)學院附屬瑞金醫(yī)院消化科張?zhí)煊钺t(yī)師等的大力支持,受到國家自然科學基金項目,、中國博士后科學基金及上海市科委揚帆計劃等資助,。
原文鏈接:https://www.cell.com/molecular-cell/fulltext/S1097-2765(20)30945-X
撰稿:胡志林
編輯:馮昫皎
審核:鄒強、方麗娟
 滬公網安備 31009102000053號 滬ICP備18007527號-1 郵箱:[email protected]
滬公網安備 31009102000053號 滬ICP備18007527號-1 郵箱:[email protected] 滬公網安備 31009102000053號 滬ICP備18007527號-1 郵箱:[email protected]
滬公網安備 31009102000053號 滬ICP備18007527號-1 郵箱:[email protected]