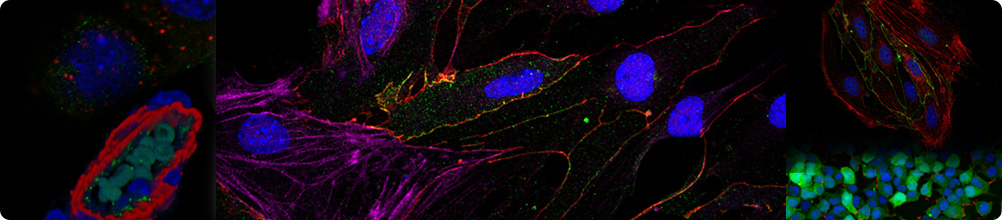
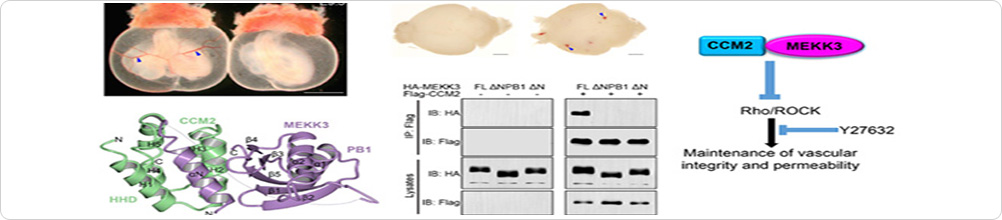
(圖1. m6A維持Treg細(xì)胞的抑制性功能,。A)Treg細(xì)胞特異性敲除Mettl3/m6A后,,小鼠自發(fā)嚴(yán)重的自身免疫疾病,。B)m6A敲除的Treg細(xì)胞在體外共培養(yǎng)抑制性功能檢測實(shí)驗(yàn)中完全喪失抑制性功能,。C)RNA-Seq發(fā)現(xiàn)Socs基因在m6A敲除Treg細(xì)胞中上調(diào),并隨著年齡的增加有上升的趨勢,。D)phospho-Kinase芯片檢測發(fā)現(xiàn)m6A敲除細(xì)胞中的IL-2-STAT5信號通路受損,。)
2018年1月5日上海交通大學(xué)醫(yī)學(xué)院上海市免疫學(xué)研究所李華兵課題組在國際著名期刊Cell Research上在線發(fā)表了題為“m6A mRNA methylation sustains Treg suppressive functions”的研究論文,發(fā)現(xiàn)RNA m6A表觀遺傳修飾可以調(diào)控Treg細(xì)胞的抑制功能及相關(guān)機(jī)制,。
m6A(N6-腺苷甲基化修飾)是最豐富,、分布最廣泛的mRNA化學(xué)修飾,李華兵研究員在2017年8月在Nature雜志發(fā)表了題為“m6A mRNA methylation controls T cell homeostasis by targeting the IL-7/STAT5/SOCS pathways”的研究論文,,首次報(bào)道了m6A修飾促進(jìn)SOCS家族mRNA降解,,從而調(diào)控IL-7/STAT5信號通路介導(dǎo)的na?ve CD4 T細(xì)胞穩(wěn)態(tài)增殖及分化過程,。在這一工作的基礎(chǔ)上,李華兵研究組發(fā)現(xiàn)調(diào)節(jié)性T細(xì)胞(Treg)特異性缺失m6A關(guān)鍵甲基轉(zhuǎn)移酶Mett3的小鼠,,在離乳(3-4周齡)之后會逐漸發(fā)生淋巴結(jié)腫大,、脾臟腫大、炎癥因子表達(dá)上調(diào),、毛發(fā)脫落等嚴(yán)重的自身免疫性疾病,,表明m6A mRNA甲基化修飾對Treg細(xì)胞行駛抑制性功能至關(guān)重要,。進(jìn)一步的研究顯示,,METTL3介導(dǎo)的m6A修飾并不影響Treg細(xì)胞在幼鼠中的發(fā)育過程,但是在離乳后逐漸接觸外界抗原過程中,,Mett3敲除的Treg細(xì)胞總數(shù)顯著減少并且基因表達(dá)譜變的紊亂,,其抑制功能顯著降低。這在體外及體內(nèi)細(xì)胞抑制實(shí)驗(yàn)?zāi)P椭械玫竭M(jìn)一步驗(yàn)證,。進(jìn)一步的結(jié)果發(fā)現(xiàn),,METTL3缺失的Treg細(xì)胞在受到IL-2信號刺激后,其STAT5磷酸化顯著下調(diào),,表明METTL3介導(dǎo)的m6A修飾的缺失,,引起Socs家族mRNA的上調(diào),并抑制了對Treg行駛功能至關(guān)重要的IL-2-STAT5信號通路,。
調(diào)節(jié)性T細(xì)胞對于維持體內(nèi)免疫系統(tǒng)的穩(wěn)態(tài)至關(guān)重要,。該研究揭示了體內(nèi)m6A甲基化修飾對Treg細(xì)胞抑制功能的關(guān)鍵調(diào)控作用,進(jìn)一步驗(yàn)證了m6A功能的特異性,,為基于Treg細(xì)胞的自身免疫性疾病等的治療提供了重要的潛在靶點(diǎn),。基于m6A去甲基化酶以及甲基化識別蛋白在免疫系統(tǒng)中的體內(nèi)功能還有待于將來進(jìn)一步的研究以便理清這一領(lǐng)域內(nèi)的爭議,。
上海交通大學(xué)醫(yī)學(xué)院上海市免疫學(xué)研究所李華兵課題組的博士后童吉宇和章婷,、來自于暨南大學(xué)在Richard Flavell實(shí)驗(yàn)室訪學(xué)的曹廣超博士在李華兵研究員和Flavell教授的共同指導(dǎo)下合作完成了這一工作。Stanford的Howard Chang,,中科大的朱書,,復(fù)旦的李華斌,以及上海市免疫所的李斌,、陳磊和蘇冰教授們參與了這一研究工作,。李華兵研究員和Richard Flavell教授為本文共同通訊作者。此項(xiàng)研究獲得了上海市高校特聘教授計(jì)劃,、國家自然科學(xué)基金委的資助,。
論文鏈接:
https://www.nature.com/articles/cr20187
李華兵研究員及課題組簡介:
李華兵,研究員,博士生導(dǎo)師,,上海市免疫學(xué)研究所2017年海外引進(jìn)課題組長(PI),。2002年和2005年本科和碩士畢業(yè)于南開大學(xué),2011年博士畢業(yè)于新澤西州立大學(xué),。2012年-2017年在美國耶魯大學(xué)Richard Flavell院士實(shí)驗(yàn)室作博士后從事T細(xì)胞RNA表觀遺傳修飾以及炎癥相關(guān)研究工作,,2017年8月加入上海交通大學(xué)醫(yī)學(xué)院上海市免疫學(xué)研究所,擔(dān)任表觀遺傳免疫學(xué)課題組長(PI),。
在表觀遺傳學(xué)和T 細(xì)胞生物學(xué)領(lǐng)域,,李華兵研究員作為第一作者,共同第一作者和共同通訊作者已在Nature, Science等國際一流期刊發(fā)表研究論文10 余篇,。2017年入選上海高校特聘教授,、國家海外青年高層次人才計(jì)劃,以及國家自然科學(xué)基金委重大研究計(jì)劃培育項(xiàng)目支持,。李華兵課題組主要從事免疫學(xué)中的表觀遺傳調(diào)控機(jī)制的研究,,以基因編輯小鼠的免疫疾病模型為基礎(chǔ),集中關(guān)注在機(jī)體免疫反應(yīng)中RNA層面的表觀修飾過程以及RNA結(jié)合蛋白的生理和分子生物學(xué)功能,,通過前沿的高通量篩選方法,,鑒定出調(diào)控免疫反應(yīng)的重要分子靶標(biāo),為開發(fā)腸道炎癥,,自身免疫疾病以及腫瘤的治療藥物提供重要理論依據(jù),。
 滬公網(wǎng)安備 31009102000053號 滬ICP備18007527號-1 郵箱:[email protected]
滬公網(wǎng)安備 31009102000053號 滬ICP備18007527號-1 郵箱:[email protected]