近日,Cell子刊《STAR Protocols》在線發(fā)表了上海交通大學醫(yī)學院公共衛(wèi)生學院王慧教授和單細胞組學與疾病研究中心何牮副研究員聯(lián)合發(fā)表的題為“Isolation of single cells from human hepatoblastoma tissues for whole-exome sequencing”的論文。

該論文提出和展示了一個簡單的方案來分離單細胞并進行單細胞全外顯子組測序。該策略結合了單細胞處理和單細胞外顯子組測序,能夠提高外顯子組的覆蓋率和低豐度變異的檢出率,同時降低實驗的時間和人力成本。在此之前,團隊圍繞單細胞測序技術中存在的一系列瓶頸問題,結合單細胞(核)分離獲取及單細胞核測序技術,已申請多項發(fā)明專利,助力單細胞多組學技術的發(fā)展。
在本研究中,作者詳細闡述了利用單細胞外顯子組測序技術研究肝母細胞瘤腫瘤微環(huán)境的實驗方案。通過將單細胞處理與全外顯子組測序相結合,創(chuàng)新性地開發(fā)了單細胞全外顯基因組測序技術,詳細描述了包括單細胞分選、全基因組擴增、擴增均勻性評估和全外顯子文庫構建乃至測序分析所涉及的一系列步驟。這一工作將多重置換擴增技術(MDA)與基因組多位點qPCR檢測結合,在外顯子組捕獲之前就排除有潛在擴增偏倚風險的單個細胞樣本,最大可能地保證了擴增均一性、大幅提升基因組覆蓋度。該方案相對于傳統(tǒng)的單細胞全基因組測序,可提升腫瘤中的低頻突變檢出率,提高研究的解析度,有助于揭示腫瘤遺傳異質性等研究。
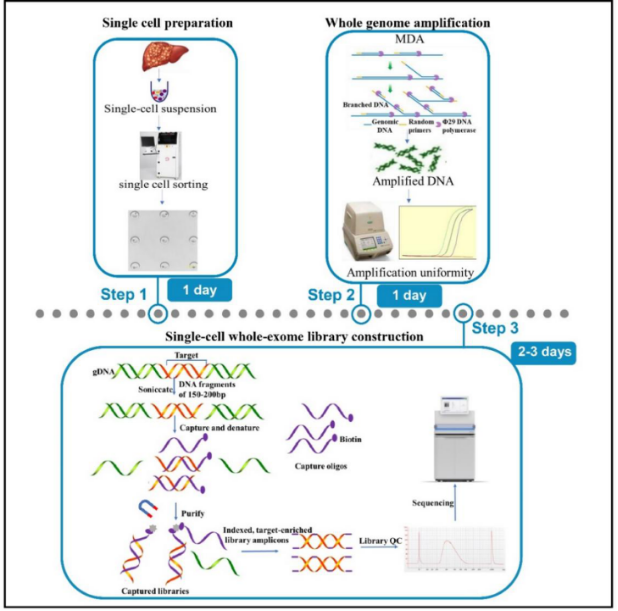
綜上所述,該論文系統(tǒng)性介紹了利用肝母細胞瘤進行單細胞全外顯子組測序的詳細流程,并通過對文庫進行質檢以及測序分析對該實驗方案的有效性進行了評價,確立了該方案在檢測人類疾病的低頻突變、揭示疾病遺傳異質性等方面的穩(wěn)定性及重要性,為疾病演進的研究以及臨床診斷和治療提供有效的參考及指導。同時該研究方案提供了實驗過程中的注意事項與常見問題解決方案,并提供了詳細的實驗相關試劑耗材,對于后續(xù)發(fā)展及推廣應用奠定基礎。
交大醫(yī)學院公共衛(wèi)生學院院長王慧教授為該論文的通訊作者,單細胞組學與疾病研究中心基因組學平臺主任何牮副研究員和孟梅為該論文的共同第一作者。該工作獲得了國家重點研發(fā)計劃(2018YFC2000700,2022YFD2101500,2022YFD2101503)、國家自然科學基金(82030099)、上海市科學技術委員會(22DZ2303000)、高水平地方大學創(chuàng)新研究團隊等資助。
據(jù)悉,基因組測序技術已成為研究疾病分子機制和遺傳特性的常規(guī)手段,隨著技術的進步,單細胞基因組測序技術成為提高研究解析度的首選手段。但目前報道的單細胞全基因測序技術普遍存在測序數(shù)據(jù)量大,測序深度低且覆蓋度低, 數(shù)據(jù)解讀難度大,錯誤率高等缺點,并且其難以區(qū)分真正的生物變異和技術偽影,不利于深度挖掘低豐度變異,且其昂貴的價格限制了其在大規(guī)模高通量單細胞研究中的應用。此外,由于約85%的人類疾病相關基因都集中于占基因組約2%的外顯子部分,因此,積極地開發(fā)高分辨率、高檢出率、低成本的單細胞外顯子組測序技術將大幅提高研究效能。
原文鏈接:https://www.sciencedirect.com/science/article/pii/S2666166723000102