近日,,著名學(xué)術(shù)期刊Advanced Materials發(fā)表了上海交通大學(xué)公共衛(wèi)生學(xué)院宋海云研究員,、化學(xué)化工學(xué)院樊春海院士與西安交通大學(xué)藥學(xué)院張繼業(yè)教授團(tuán)隊(duì)題為“Composite Hydrogel for Spatiotemporal Lipid Intervention of Tumor Milieu”的研究成果,。該研究構(gòu)建了一種響應(yīng)腫瘤微環(huán)境的智能型復(fù)合水凝膠,,靶向腫瘤組織內(nèi)不同的細(xì)胞類型分別遞送載藥納米粒子和游離藥物,并結(jié)合近紅外光熱治療,,通過(guò)對(duì)腫瘤微環(huán)境的時(shí)空脂質(zhì)干預(yù)發(fā)展了新的腫瘤免疫療法,。
免疫原性細(xì)胞死亡(ICD)在腫瘤免疫治療中扮演著不可或缺的角色。然而,,癌細(xì)胞中存在的雙重抗脂質(zhì)氧化機(jī)制可以抑制ICD的產(chǎn)生,,而免疫抑制細(xì)胞中存在的異常脂質(zhì)代謝也嚴(yán)重妨害了免疫系統(tǒng)對(duì)ICD的感知。該研究發(fā)現(xiàn)中空介孔硫化銅納米粒子(CuS NPs)具有抑制谷胱甘肽過(guò)氧化物酶4(GPX4)的內(nèi)在生物學(xué)特性,,當(dāng)其負(fù)載鐵死亡抑制蛋白1(FSP1)的抑制劑(iFSP1)時(shí),,能平行地阻斷癌細(xì)胞內(nèi)兩條抗脂質(zhì)氧化的信號(hào)通路,再結(jié)合近紅外輻射后可以三效合一地促進(jìn)癌細(xì)胞的脂質(zhì)過(guò)氧化和增強(qiáng)ICD,。研究人員進(jìn)一步制備了一種腫瘤微環(huán)境響應(yīng)型水凝膠來(lái)共同遞送靶向癌細(xì)胞的CuS NPs和靶向免疫抑制細(xì)胞的脂質(zhì)吸收抑制劑(SSO),,對(duì)腫瘤內(nèi)的不同細(xì)胞群進(jìn)行時(shí)空可控性的脂質(zhì)干預(yù)。負(fù)載iFSP1的CuS NPs通過(guò)促進(jìn)脂質(zhì)過(guò)氧化產(chǎn)生ICD信號(hào),,SSO通過(guò)重塑脂質(zhì)代謝恢復(fù)免疫監(jiān)測(cè),,二者協(xié)同誘導(dǎo)先天性和適應(yīng)性免疫并抑制腫瘤的生長(zhǎng)、復(fù)發(fā)及轉(zhuǎn)移,,從而發(fā)展了一種新型的基于脂質(zhì)干預(yù)的腫瘤免疫代謝療法(圖1),。
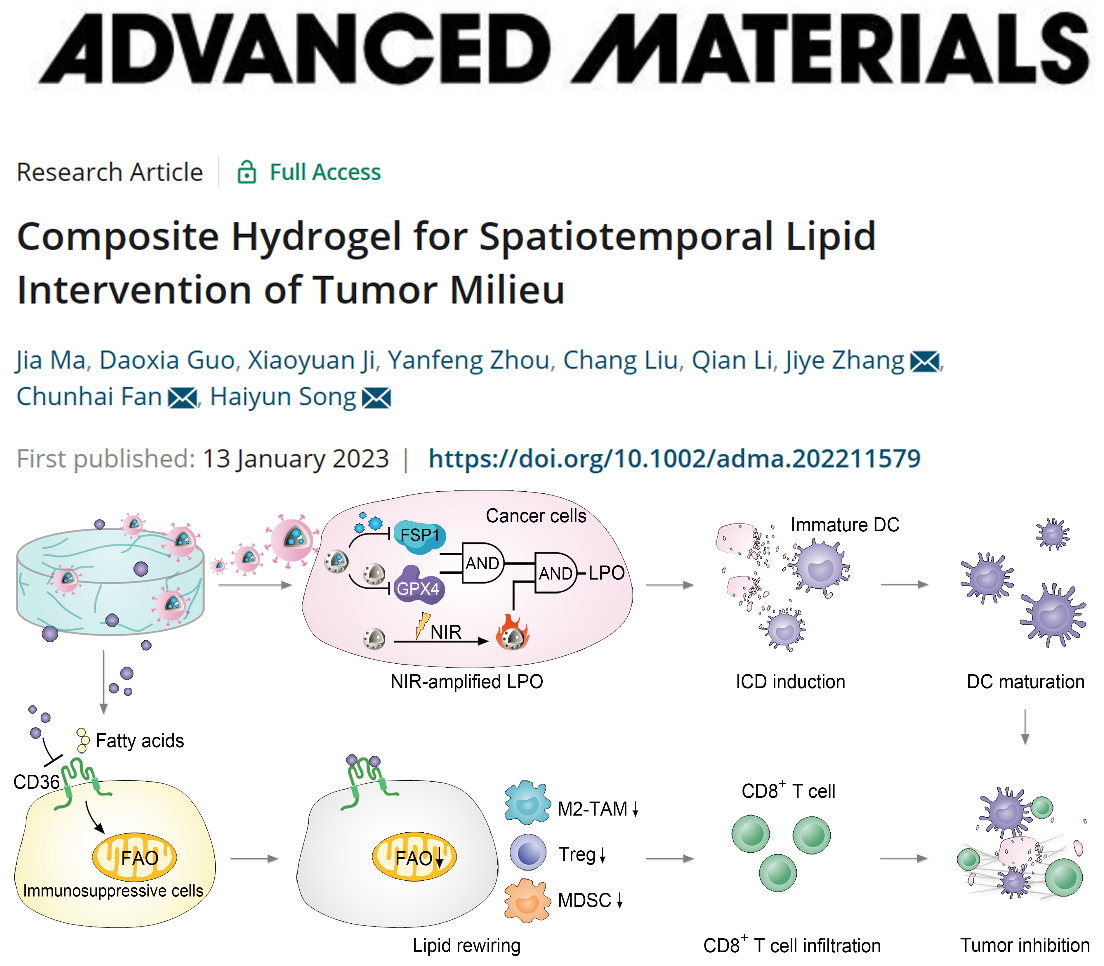
圖1復(fù)合水凝膠抗腫瘤策略示意圖。圖片來(lái)源:Adv. Mater.
鐵死亡是一種由脂質(zhì)過(guò)氧化引起的ICD,。當(dāng)人們熟知的system xc-/glutathione/GPX4抗氧化信號(hào)通路被抑制時(shí),,會(huì)導(dǎo)致脂質(zhì)過(guò)氧化物的累積。然而這種情況下,,許多種類的癌細(xì)胞可以通過(guò)一條平行的FSP1/NAD(P)H抗氧化途徑來(lái)避免鐵死亡的產(chǎn)生,,從而減弱了ICD信號(hào)的強(qiáng)度和腫瘤免疫療法的療效。本研究中,,靶向腫瘤細(xì)胞的CuS NPs自身固有的抑制GPX4特性與負(fù)載的iFSP1平行誘導(dǎo)脂質(zhì)過(guò)氧化作用,。同時(shí),CuS NPs的光熱效應(yīng)可協(xié)同增強(qiáng)ICD,。
除癌細(xì)胞自主性地限制ICD外,,癌細(xì)胞特有的代謝特性創(chuàng)造了具有免疫抑制性的腫瘤微環(huán)境(TME),從而削弱免疫系統(tǒng)對(duì)ICD信號(hào)的感知,,導(dǎo)致免疫逃逸,。TME中產(chǎn)生大量的脂質(zhì)代謝產(chǎn)物并在M2型腫瘤相關(guān)巨噬細(xì)胞(M2-TAMs)、髓源抑制性細(xì)胞(MDSCs)和調(diào)節(jié)性T(Treg)細(xì)胞等免疫抑制細(xì)胞中異常積累,,促進(jìn)其分化和發(fā)揮免疫抑制功能,。該類細(xì)胞所共有的特征是細(xì)胞表面高表達(dá)CD36受體,負(fù)責(zé)攝取脂質(zhì)作為細(xì)胞主要能量來(lái)源,。因此,,阻斷脂質(zhì)攝取可通過(guò)代謝重編程限制這類免疫抑制性細(xì)胞的功能,恢復(fù)免疫監(jiān)測(cè),。在本研究中,,水凝膠中釋放的SSO可靶向M2-TAMs、MDSCs和Treg細(xì)胞表面的CD36受體,,阻斷脂質(zhì)攝取,,重塑細(xì)胞功能,解除TME的免疫抑制,,從而促進(jìn)細(xì)胞毒性T淋巴細(xì)胞的浸潤(rùn)(圖2),。
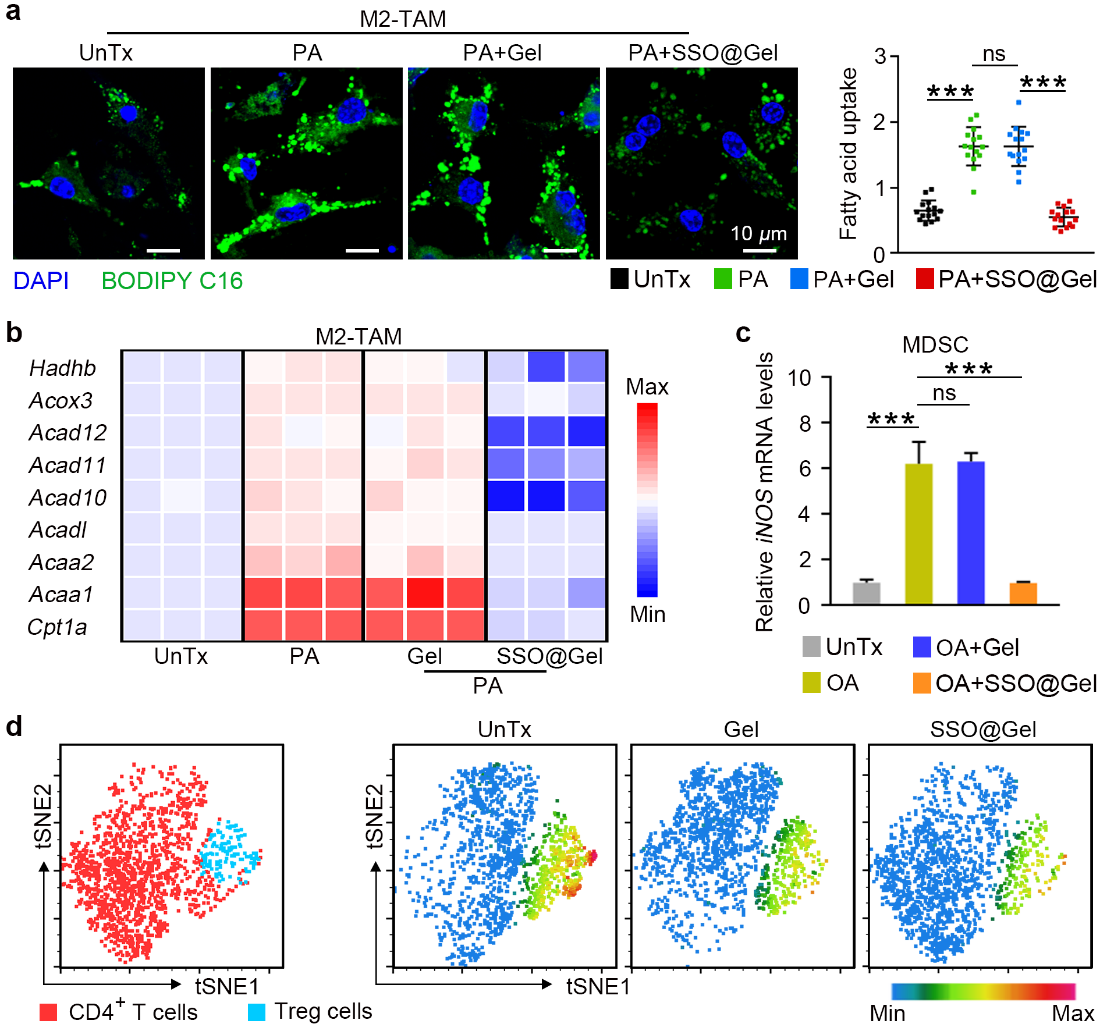
圖2 水凝膠通過(guò)脂質(zhì)干預(yù)重塑免疫抑制細(xì)胞。圖片來(lái)源:Adv. Mater.
在小鼠三陰性乳腺癌模型中,,同時(shí)遞送CuS NPs和SSO的復(fù)合水凝膠通過(guò)雙管齊下的方法對(duì)腫瘤細(xì)胞和免疫抑制細(xì)胞進(jìn)行調(diào)控,,分別增強(qiáng)ICD信號(hào)和ICD感知,協(xié)同觸發(fā)先天性和適應(yīng)性免疫以抑制腫瘤的發(fā)展進(jìn)程,。此外,,在小鼠乳腺癌切除模型中,,該復(fù)合水凝膠能夠有效抑制腫瘤的術(shù)后復(fù)發(fā)和轉(zhuǎn)移。這項(xiàng)研究提出了一種時(shí)空干預(yù)腫瘤微環(huán)境脂質(zhì)代謝的新策略,,為腫瘤的免疫療法提供了一種全新的思路和方法,。
上海交通大學(xué)公共衛(wèi)生學(xué)院宋海云研究員、化學(xué)化工學(xué)院樊春海院士和西安交通大學(xué)藥學(xué)院張繼業(yè)教授為該文的共同通訊作者,。西安交通大學(xué)博士研究生馬佳,、上海交通大學(xué)博士研究生郭道霞和副研究員季曉媛為該論文的并列第一作者。
原文鏈接:https://onlinelibrary.wiley.com/doi/10.1002/adma.202211579