12月6日,國際腫瘤免疫治療學會官方雜志《Journal for ImmunoTherapy of Cancer》在線發(fā)表了上海交通大學醫(yī)學院公共衛(wèi)生學院王慧/李曉光聯(lián)合團隊題為“Caspase-9 inhibition triggers Hsp90-based chemotherapy-mediated tumor intrinsic innate sensing and enhances antitumor immunity”的研究論文,該研究揭示了化療藥物誘導的含半胱氨酸的天冬氨酸蛋白水解酶(Caspase)信號是限制腫瘤先天免疫感知的主要內在障礙,而阻斷Caspase 9信號可顯著增強HSP90化療藥物誘導的Ⅰ型干擾素(IFN-I)產生和先天免疫應答,聯(lián)合抗PD-L1免疫治療可實現(xiàn)腫瘤完全消退,為腫瘤治療提供了潛在的創(chuàng)新策略。
傳統(tǒng)的癌癥治療方法,例如化療、放療和靶向治療,通常通過直接殺傷腫瘤細胞的方式來抑制癌癥的生長和擴散。這些治療方法通常會觸發(fā)Caspase信號,導致腫瘤細胞發(fā)生凋亡,并同時引發(fā)免疫系統(tǒng)的沉默反應。然而,目前仍不清楚激活的Caspase是否是化療藥物引起免疫沉默的主要原因,以及它們在化療藥物引發(fā)細胞死亡中是否是不可或缺的。為了解決這一問題,研究團隊建立了一個IFN-I免疫應答的高通量體外篩選系統(tǒng),并利用包含1214種化療藥物的抗癌藥物庫進行了驗證實驗,結果表明抑制Caspase信號能夠廣泛提高化療藥物引發(fā)的IFN先天免疫信號,并促進IFN-I的產生。在這項無偏倚篩選中,研究人員發(fā)現(xiàn)IFN-I應答排名前十的候選藥物中有8種是Hsp90抑制劑(見圖1),凸顯了Hsp90作為調節(jié)先天免疫信號重要靶點的潛在優(yōu)勢和重要性。
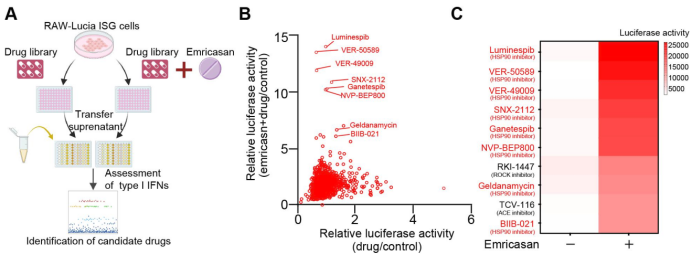
圖1 阻斷Caspase顯著促進化療藥物誘導的Ⅰ型干擾素的產生
機制研究發(fā)現(xiàn),Hsp90抑制劑能夠激活內源性凋亡并導致線粒體DNA的釋放,從而引發(fā)cGAS-STING-IRF3依賴的DNA感應信號激活。然而,內源性凋亡會觸發(fā)Caspase3/7/9信號并介導cGAS/STING/TBK1的剪切,阻礙了由線粒體DNA介導的先天免疫感知。在泛Caspase抑制劑存在或Caspase 9(內源性凋亡關鍵中介因子)敲除狀態(tài)下,Hsp90抑制劑顯著激活了Ⅰ型干擾素信號;敲除Caspase 8(外源性凋亡的關鍵執(zhí)行因子)并未發(fā)現(xiàn)這一現(xiàn)象。有趣的是,體內外實驗證實抑制內源性Caspase通路并沒有影響Hsp90抑制劑引起的細胞死亡,表明激活內源性Caspase通路可能不是以HSP90為靶點的化療引起的細胞死亡及隨后凋亡細胞清除的必要因素。
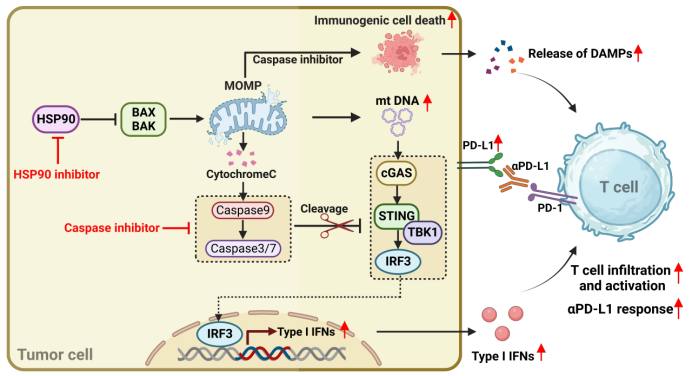
圖2 阻斷Caspase增強Hsp90抑制劑抗腫瘤策略示意圖
在小鼠腫瘤模型中,阻斷Caspase信號顯著增強了腫瘤的免疫原性并激活了先天免疫反應,導致顯著的抗腫瘤效果。這種免疫激活的能力明顯增強了腫瘤對免疫檢查點抑制劑αPD-L1的藥物敏感性,并實現(xiàn)了腫瘤的完全消退(見圖2)。這項研究提出了通過靶向抑制Caspase來增強現(xiàn)有抗癌藥物治療的策略。它挑戰(zhàn)了傳統(tǒng)通過激活Caspase誘導腫瘤細胞凋亡的治療方法,為提升化療的免疫原性提供了新的思路和方法。
上海交通大學醫(yī)學院公共衛(wèi)生學院博士李錦陽、韓筱俁和博士后孫馬鈺為該論文共同第一作者。公共衛(wèi)生學院王慧教授和李曉光研究員為該論文的共同通訊作者。該研究得到了國家重點研發(fā)計劃和國家自然科學基金等項目的資助。
原文鏈接:https://jitc.bmj.com/content/11/12/e007625