細(xì)胞內(nèi)代謝穩(wěn)態(tài)對于造血干細(xì)胞的自我更新與分化至關(guān)重要。雖然造血干細(xì)胞在靜息狀態(tài)下通常以糖酵解為主要代謝途徑,但精密調(diào)控的線粒體代謝活性也是造血干細(xì)胞穩(wěn)態(tài)平衡的維持所必需的(Filippi et al. 2019;Yu et al. 2013)。研究表明,敲除鐵硫簇蛋白顯著破壞線粒體呼吸鏈的功能從而引起造血干細(xì)胞庫的衰竭(Ansó et al. 2013)。異常激活線粒體未折疊蛋白反應(yīng)與線粒體應(yīng)激損害造血干細(xì)胞的靜息狀態(tài),導(dǎo)致造血干細(xì)胞的長期移植能力顯著下降(Mohrin et al. 2015)。RNA可變剪接是從同一轉(zhuǎn)錄本前體產(chǎn)生不同RNA變體的一種利于細(xì)胞節(jié)能的基因表達(dá)調(diào)節(jié)方式(Chen et al. 2009;Marasco et al. 2023)。可變剪接的調(diào)控在細(xì)胞增殖、分化、代謝、衰老以及死亡等多種生物學(xué)過程中發(fā)揮重要作用。參與RNA可變剪接的一些核心組分通常包括小RNA及其RNA結(jié)合蛋白。多種剪接因子如Srsf2、U2af1等被報(bào)道參與胎肝或成體骨髓造血干細(xì)胞的穩(wěn)態(tài)調(diào)控(Komeno et al. 2015;Dutta et al. 2021)。剪接過程的紊亂與惡性造血也密切相關(guān),在急性髓系白血病、骨髓異常增生綜合癥患者臨床樣本中檢測到SRSF2、SF3B1、U2AF1和ZRSR2存在基因突變(Saez et al. 2017;Yoshimi et al. 2019)。但迄今為止,可變剪接如何整合調(diào)控造血干祖細(xì)胞的線粒體代謝尚未報(bào)道。
10月13日,基礎(chǔ)醫(yī)學(xué)院病理生理學(xué)系郭濱課題組與美國印第安納大學(xué)醫(yī)學(xué)院萬鈞團(tuán)隊(duì)、山西醫(yī)科大學(xué)賀杰峰團(tuán)隊(duì)合作在Cell Reports期刊上發(fā)表了題為Aspartyl-tRNA synthetase 2 orchestrates iron-sulfur metabolism in hematopoietic stem cells via fine-tuning alternative RNA splicing的研究論文。該研究發(fā)現(xiàn)線粒體氨酰tRNA合酶Dars2通過定位到造血干祖細(xì)胞的剪接體與剪接因子Srsf3等互作,調(diào)控代謝相關(guān)基因包括mtor和Slc22a17的mRNA可變剪接事件,進(jìn)而通過調(diào)控鐵硫簇代謝影響線粒體穩(wěn)態(tài)和造血干細(xì)胞庫的維持。
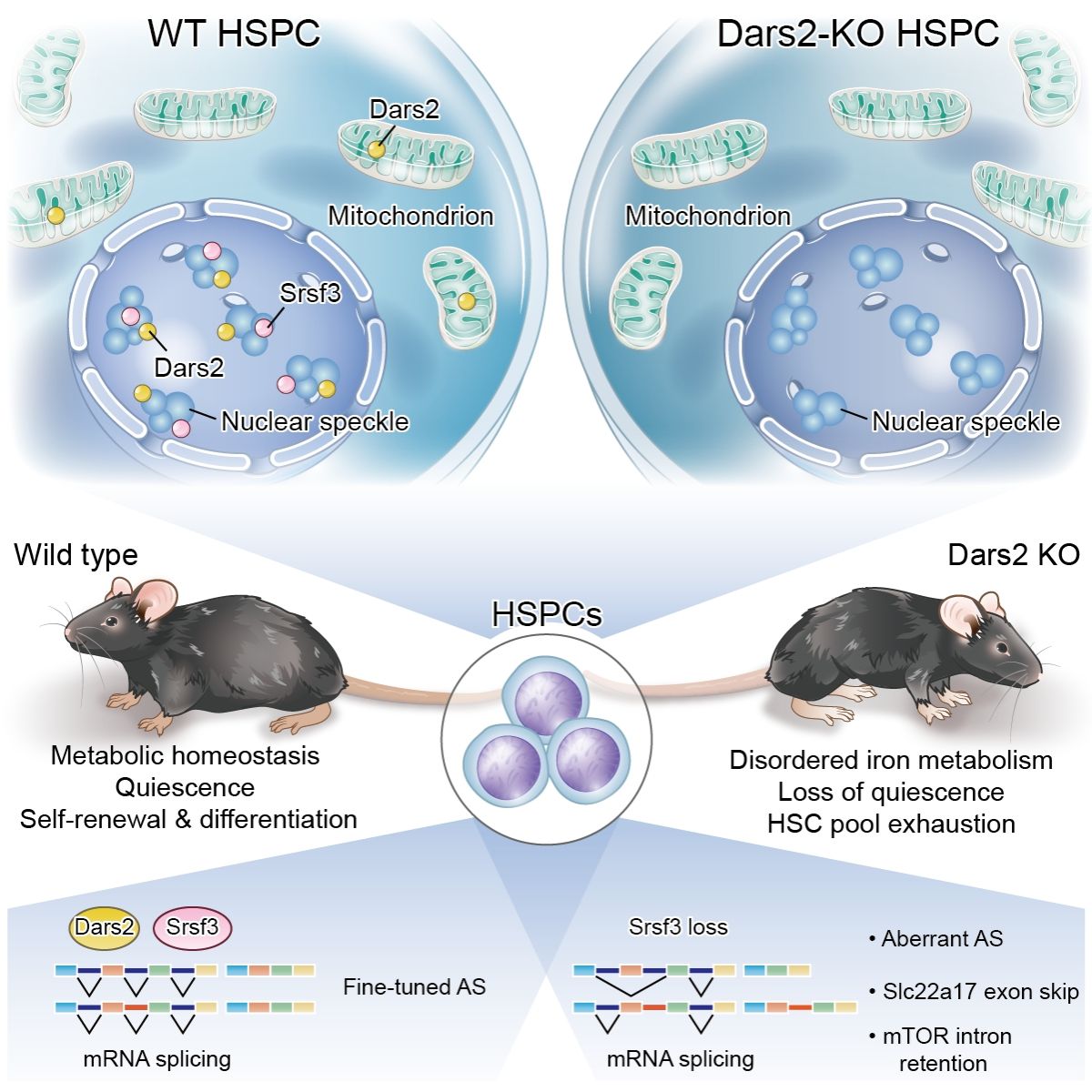
Dars2調(diào)控造血干細(xì)胞穩(wěn)態(tài)維持的機(jī)制
郭濱團(tuán)隊(duì)致力于細(xì)胞器應(yīng)激與造血系統(tǒng)再生調(diào)控機(jī)制研究。在部分前期工作基礎(chǔ)上(Leukemia 2019;J Clinic Invest 2021),該研究構(gòu)建了Dars2基因在血液系統(tǒng)的條件敲除小鼠模型,發(fā)現(xiàn)Dars2功能缺失逐步引起小鼠的造血活性下調(diào)、嚴(yán)重貧血、造血干祖細(xì)胞庫枯竭以及小鼠死亡。Dars2的經(jīng)典功能是調(diào)控線粒體天冬氨酸與tRNA的連接從而參與線粒體基因組編碼的蛋白質(zhì)合成。前期國際上有研究報(bào)道Dars2在心肌細(xì)胞和巨噬細(xì)胞中存在不依賴于氨酰tRNA合酶活性的功能(Dogan et al. 2014;Willenborg et al. 2021)。本研究發(fā)現(xiàn),Dars2在造血干細(xì)胞中的功能缺失后并未顯著改變線粒體基因編碼的蛋白組分合成水平,提示Dars2可能通過一種新的機(jī)制調(diào)節(jié)造血干細(xì)胞的功能。研究人員進(jìn)一步進(jìn)行了非標(biāo)記定量(Lable free)蛋白質(zhì)組學(xué)分析,結(jié)果發(fā)現(xiàn)Dars2敲除的造血干祖細(xì)胞中下調(diào)最為顯著的一類蛋白是剪接因子,包括Srsf2、Srsf3、Srsf6等。通過免疫熒光與蛋白質(zhì)免疫共沉淀實(shí)驗(yàn),作者意外發(fā)現(xiàn)Dars2除了定位在線粒體,還顯著定位到造血干祖細(xì)胞中的剪接體,并與剪接因子Srsf3互作。Dars2敲除后,造血干祖細(xì)胞中Srsf3的蛋白穩(wěn)定性破壞從而導(dǎo)致其降解。通過可變剪接分析發(fā)現(xiàn),Dars2敲除的造血干祖細(xì)胞中多種代謝過程基因的RNA可變剪接事件出現(xiàn)顯著異常。其中包括一個(gè)之前在心肌細(xì)胞中被報(bào)道受Srsf3調(diào)控的mtor基因,它發(fā)生了內(nèi)含子滯留。其它剪接事件中,研究人員關(guān)注到Slc22a17基因,該基因的RNA在Dars2敲除的造血干祖細(xì)胞中出現(xiàn)了顯著的外顯子跳躍,引起讀碼框的移位,形成三個(gè)連續(xù)的終止密碼子。進(jìn)一步研究發(fā)現(xiàn),Dars2敲除的造血干祖細(xì)胞中Slc2217的啟動子活性沒有顯著改變,而mRNA水平顯著降低,提示可能發(fā)生了mRNA decay。RNA免疫共沉淀實(shí)驗(yàn)表明,Srsf3可以顯著與Slc22a17的RNA結(jié)合。Slc22a17被報(bào)道參與了一些細(xì)胞類型內(nèi)鐵穩(wěn)態(tài)的調(diào)控,敲除Dars2和敲減Slc22a17的造血干祖細(xì)胞內(nèi)的鐵含量顯著降低,蛋白組學(xué)結(jié)果顯示鐵硫簇蛋白組分表達(dá)顯著下調(diào)。鐵硫簇蛋白在線粒體呼吸鏈電子傳遞與DNA損傷修復(fù)中發(fā)揮著重要作用。研究人員發(fā)現(xiàn),Dars2敲除引起造血干祖細(xì)胞線粒體呼吸代謝活性下調(diào)和DNA損傷累積。敲減Slc22a17顯著抑制造血干祖細(xì)胞的克隆形成能力,而過表達(dá)Slc22a17能夠部分回補(bǔ)因Dars2功能缺失引起的鐵代謝紊亂和造血功能損傷。該論文揭示了第一個(gè)氨酰tRNA合酶在造血干細(xì)胞穩(wěn)態(tài)調(diào)控中的功能,報(bào)道了Dars2通過控制RNA可變剪接的方式參與線粒體代謝活性與穩(wěn)態(tài)的調(diào)控,為造血干細(xì)胞的代謝調(diào)控提供了全新視角。
基礎(chǔ)醫(yī)學(xué)院2021級博士研究生顧璇與印第安納大學(xué)醫(yī)學(xué)院萬鈞團(tuán)隊(duì)博士研究生酈凱凌為論文的共同第一作者;郭濱研究員、萬鈞教授、賀杰峰教授為論文的共同通訊作者。該研究受到科技部國家重點(diǎn)研發(fā)計(jì)劃“干細(xì)胞與轉(zhuǎn)化研究”重點(diǎn)專項(xiàng)、國家自然科學(xué)基金委重大研究計(jì)劃培育項(xiàng)目、面上項(xiàng)目以及美國血液學(xué)會GRA等資助。
原文鏈接:https://www.cell.com/cell-reports/fulltext/S2211-1247(23)01276-7