上海交通大學(xué)醫(yī)學(xué)院附屬瑞金醫(yī)院、上海血液學(xué)研究所、醫(yī)學(xué)基因組學(xué)國家重點實驗室蒙國宇教授和陳竺院士團(tuán)隊受腫瘤學(xué)權(quán)威期刊Trends in Cancer邀請,在線發(fā)表標(biāo)題為“PML nuclear body biogenesis, carcinogenesis and targeted therapy”的特邀綜述文章。該綜述從PML核體的組裝機(jī)制到PML驅(qū)動的基因組組構(gòu)以及腫瘤形成全方位探討了近期PML領(lǐng)域的突破,并提出“以PML為核心的抗腫瘤新策略”。
白血病(也稱血癌)在35歲以下人群中是發(fā)病率和死亡率排名第一的癌癥,尤其是青少年和幼兒。以急性髓系白血病為例,其患者生存率從2002-2018年沒有顯著的提高,5年生存率仍不足20%,所以改善白血病治療效果、提高病人生存率仍是我國臨床上的重大需求。該團(tuán)隊從“上海方案”出發(fā),不斷探究以PML為核心的抗腫瘤新策略,于2018年3月和2019年8月在Nature Communications雜志上連續(xù)發(fā)表“PML核體組裝機(jī)制新發(fā)現(xiàn)”,揭示了與急性髓系白血病發(fā)病相關(guān)的PML核體組裝的新機(jī)制,為后續(xù)白血病的靶向治療提供了新的思路。并提出了“癌蛋白的聚合是腫瘤發(fā)生的重要因素”的新觀點于2020年3月發(fā)表在Blood Science雜志上。
緊接著,該團(tuán)隊圍繞PML核體繼續(xù)深耕挖掘以期能夠解決眾多懸而未解的科學(xué)問題將其應(yīng)用到更多的白血病與實體瘤當(dāng)中去。自1960年科研人員從細(xì)胞的核基質(zhì)中觀察到罕見的超級組裝復(fù)合物——PML核體以來,就因其功能廣泛而廣受國內(nèi)外科學(xué)家關(guān)注。然而PML核體的組裝機(jī)制、其在細(xì)胞中具體功能以及與腫瘤發(fā)生的關(guān)系至今仍不清楚。在這篇綜述中,作者提出了PML核體組裝新機(jī)制;歸納總結(jié)了PML核體的新功能即PML核體對人類基因組組構(gòu)有重要影響;探討了PML在不同腫瘤發(fā)生中的雙重作用。旨在為基于PML核體的腫瘤靶向治療提供新的思路與啟發(fā)。

在這篇文章中,蒙國宇教授提出PML在溶液中是動態(tài)、有規(guī)律的聚合,從而構(gòu)成PML SUMOylation修飾的基礎(chǔ),逐步組裝成這個超級組裝復(fù)合體。并且,PML核體作為一個無膜核結(jié)構(gòu)暗示其在溶液中的聚合很可能是一種相分離的過程,同PML以及伙伴蛋白形成活性網(wǎng)絡(luò)調(diào)控PML核體強(qiáng)大的生物學(xué)功能。此外,PML核體在基因組組構(gòu)中的新功能值得進(jìn)一步探究,PML核體位于核內(nèi)染色質(zhì)之間,可作為多種DNA相關(guān)事件發(fā)生的“倉庫”,且能夠在DNA合成期間保持基因組的完整性。這提示靶向PML核體進(jìn)而調(diào)節(jié)人類基因組組構(gòu)是一種潛在的腫瘤靶向新策略。更重要的是,在人類癌癥中,PML被證明扮演著雙重角色。在許多癌癥病人的組織中PML蛋白表達(dá)下調(diào),說明PML作為腫瘤抑制子下調(diào)后會啟動癌癥發(fā)生;近年來越來越多研究表明在慢性粒細(xì)胞白血病以及膠質(zhì)瘤、乳腺癌等實體瘤中PML可以作為腫瘤啟動因子導(dǎo)致癌癥發(fā)生。這提示在白血病以及實體瘤的治療中,PML可以作為一個潛在的靶點。
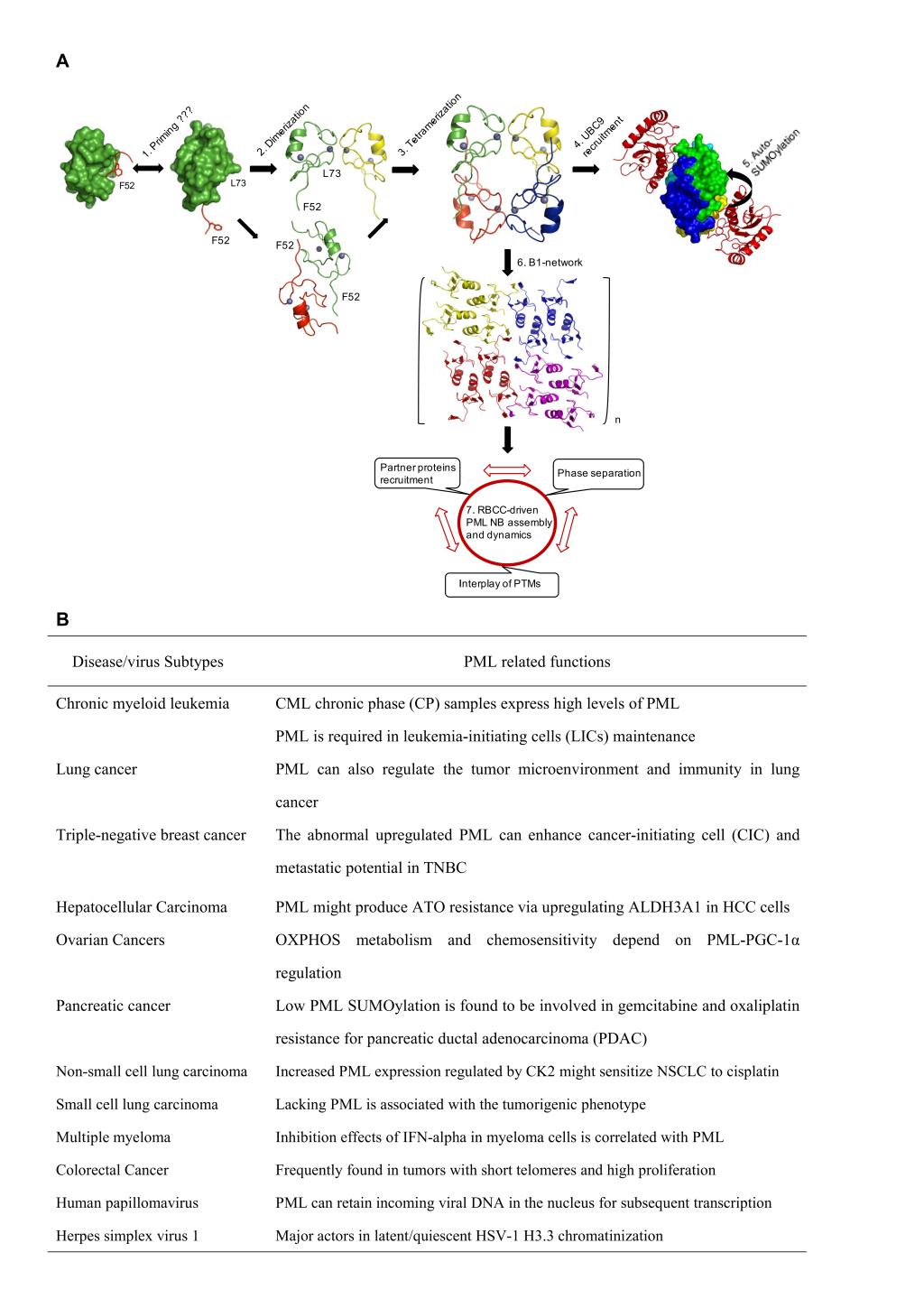
綜上所述,該團(tuán)隊在這篇文章中為此領(lǐng)域的發(fā)展指明了新的研究方向,并且站在原“上海方案”的高度上,獨辟蹊徑地提出“以PML核體為核心的抗腫瘤新策略”,以期將砷劑靶向治療拓展到AML、CML等其他類型白血病和乳腺癌、膠質(zhì)瘤等實體腫瘤的治療當(dāng)中,建立以PML核體為核心的靶向治療新策略。
蒙國宇教授和陳竺院士是文章的通訊作者,李玉文博士和馬曉丹博士是文章的第一作者。該研究獲得國家自然科學(xué)基金、上海市科委重點、教委高峰高原基金、東方學(xué)者基金等項目、國家蛋白質(zhì)中心及上海同步輻射光源BL19U2、BL17U1等線站的支持。
文章鏈接:https://doi.org/10.1016/j.trecan.2020.05.005

