7月24日,附屬新華醫(yī)院婦產(chǎn)科汪希鵬團隊與北京大學(xué)生物醫(yī)學(xué)前沿創(chuàng)新中心(BIOPIC)張澤民團隊以及上海交通大學(xué)醫(yī)學(xué)院上海市免疫學(xué)研究所博士后李子逸等合作在Nature Cancer雜志上在線發(fā)表了題為“Single-cell analyses implicate ascites in remodeling the ecosystems of primary and metastatic tumors in ovarian cancer”的研究論文,指出腹水中記憶T細胞對腫瘤原發(fā)灶及網(wǎng)膜轉(zhuǎn)移灶免疫微環(huán)境的關(guān)鍵重塑作用,,并揭示了腫瘤組織和腹水中巨噬細胞功能表型和發(fā)育起源的異質(zhì)性,,為深入理解卵巢癌進展中惡性腹水的關(guān)鍵作用以及探索靶向腫瘤腹水的免疫治療策略提供了全新的思路和數(shù)據(jù)平臺,。

卵巢癌是病死率最高的婦科腫瘤,,嚴重威脅著女性的生殖健康,。卵巢癌病理亞型中最常見的是高級別漿液性卵巢癌(HGSOC),超過75%的HGSOC患者首次發(fā)現(xiàn)時病情已進展至晚期,并伴有廣泛的惡性腹水和網(wǎng)膜轉(zhuǎn)移[1],。盡管大多數(shù)患者能從手術(shù)+鉑類化療+貝伐珠單抗的聯(lián)合治療中顯著獲益,但仍有一部分患者的整體生存率并沒有得到明顯改善,。此外,,卵巢癌腹水中的成纖維細胞可以通過激活腫瘤細胞的 JAK-STAT信號通路進而促進腫瘤生長[2]。因此,,一個涵蓋多組織位點的高分辨率單細胞圖譜對于理解卵巢癌,,特別是其網(wǎng)膜轉(zhuǎn)移灶及腹水的免疫微環(huán)境極為重要。
研究團隊對來自14例上皮性卵巢癌患者的原發(fā)灶,、網(wǎng)膜轉(zhuǎn)移灶,、腹水、外周血以及盆腔淋巴結(jié)等39個樣本進行了10X Genomics單細胞轉(zhuǎn)錄組測序和T細胞受體測序,。通過對卵巢癌個體5個部位樣本內(nèi)細胞類群相對比例的比較,,結(jié)果發(fā)現(xiàn),盡管腹水中普遍可以檢測到腫瘤細胞的存在,,但腹水環(huán)境并未呈現(xiàn)出如腫瘤組織內(nèi)部的免疫抑制性狀態(tài),。腹水中富集的記憶T細胞也是腫瘤浸潤的終末態(tài)T細胞的重要來源,比如,,腹水中的GZMK+Tem細胞可以浸潤至腫瘤組織中并直接轉(zhuǎn)化為Tex細胞,,揭示了腹水在塑造腫瘤微環(huán)境中發(fā)揮的關(guān)鍵作用。此外,,通過比較腫瘤及腹水中富集的巨噬細胞的基因表達特征,,作者發(fā)現(xiàn)組織微環(huán)境和細胞發(fā)育來源共同影響著巨噬細胞的功能表型。最后,,研究團隊發(fā)現(xiàn)治療前樣本中原發(fā)灶的VCAM+內(nèi)皮細胞,、腹水中MAIT細胞(mucosal-associated invariant T cells)和cDC1細胞可以提示HGSOC患者對鉑類化療的敏感性,有望作為預(yù)測卵巢癌鉑類化療反應(yīng)性的新指標,。
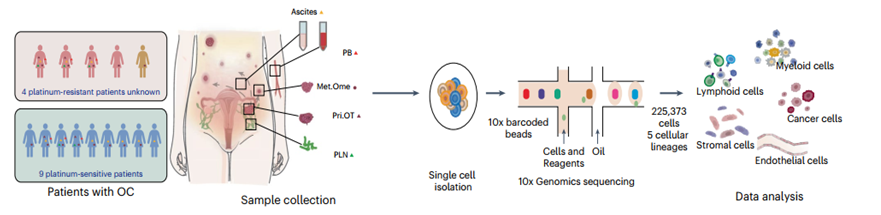
圖1:本研究的實驗設(shè)計和流程圖
上海交通大學(xué)醫(yī)學(xué)院附屬新華醫(yī)院博士研究生鄭小翠,、王昕婧,復(fù)旦大學(xué)附屬腫瘤醫(yī)院婦科醫(yī)師程璽為該論文并列第一作者,。上海交通大學(xué)醫(yī)學(xué)院附屬新華醫(yī)院汪希鵬教授,,北京大學(xué)生物醫(yī)學(xué)前沿創(chuàng)新中心(BIOPIC)張澤民教授以及上海交通大學(xué)醫(yī)學(xué)院上海市免疫學(xué)研究所博士后李子逸為本文的共同通訊作者,上海市免疫學(xué)研究所Florent Ginhoux團隊的劉兆遠研究員,,郭薇博士后等為本研究提供了重要幫助,。

