
8月,上海交通大學(xué)醫(yī)學(xué)院附屬瑞金醫(yī)院、上海血液學(xué)研究所、醫(yī)學(xué)基因組學(xué)國家重點(diǎn)實(shí)驗(yàn)室蒙國宇教授團(tuán)隊(duì)在Nature Communications上發(fā)表題目為B1 oligomerization regulates PML nuclear body biogenesis and leukemogenesis的最新研究成果。這些系列研究發(fā)現(xiàn)在PML-RING結(jié)構(gòu)域介導(dǎo)的四聚的基礎(chǔ)上,PML-B1 box結(jié)構(gòu)域能夠介導(dǎo)一種前所未有的寡聚化模式,進(jìn)而形成PML核體。同時(shí),研究者通過轉(zhuǎn)基因小鼠和單細(xì)胞技術(shù)進(jìn)一步證實(shí)了蛋白寡聚在白血病發(fā)病的重要意義,為后續(xù)的靶向治療提供新的思路。

蛋白聚合影響癌癥發(fā)生這一現(xiàn)象曾被多次報(bào)道,比如癌蛋白NPM-RARa和Stat5b-RARa寡聚化被報(bào)道與細(xì)胞無限增殖以及疾病發(fā)生至關(guān)重要;原癌基因蛋白erbB-2,MET和FGFR中,因蛋白聚合而增強(qiáng)的、獲得性的致癌作用在腫瘤生長以及癌癥發(fā)展中同樣曾被觀察到;在白血病中,這種聚合現(xiàn)象也廣泛存在于BCR/ABL, AML1/ETO, AML1/MTG16, TEL/AML1. CBF /SMMHC, MLL/GAS7, MLL/AF1p, MLL/GEPRIN以及PAX5/PML等癌蛋白中,然而聚合影響發(fā)病的機(jī)制目前尚未明確。
蒙國宇教授團(tuán)隊(duì)曾于2018年3月在Nature Communications上發(fā)表題目為Ring tetramerization is required for nuclear body biogenesis and PML sumoylation的研究論文,該研究從分子水平上揭示了PML核體組裝機(jī)制及PML自身SUMO化修飾的結(jié)構(gòu)基礎(chǔ),并發(fā)現(xiàn)PML-RING的四聚化對急性早幼粒細(xì)胞白血病(APL)的發(fā)病及其靶向治療都有很重要的意義。

急性早幼粒細(xì)胞白血病蛋白(PML)是構(gòu)成PML核體的主要組成成分。PML核體是直徑為0.1-2 m的顆粒狀復(fù)合物附著于核基質(zhì)上,研究表明PML核體在DNA損傷反應(yīng)、細(xì)胞凋亡、細(xì)胞衰老以及血管生成等途徑中扮演著十分重要的角色。并且PML核體招募120多種不同的伙伴蛋白如DAXX、SP100、SUMO等相互作用形成“PML interactosome”,進(jìn)一步通過蛋白翻譯后修飾作用如SUMO化、磷酸化、乙酰化等顯著影響伙伴蛋白在細(xì)胞中的功能。這些把PML核體推向細(xì)胞信號通路的中心位置。
急性早幼粒細(xì)胞白血病APL曾因發(fā)病病程短并且出血嚴(yán)重被視為最兇險(xiǎn)的急性白血病。而臨床上三氧化二砷和全反式維甲酸聯(lián)合用藥的發(fā)現(xiàn)使得APL成為唯一可以治愈的白血病,故此APL的發(fā)病機(jī)理以及靶向治療機(jī)制一直是研究人員的關(guān)注熱點(diǎn),有待為其他白血病和腫瘤治療提供良好借鑒。APL的發(fā)病分子機(jī)制是第15和17號染色體發(fā)生易位形成PML/RAR 融合癌基因,一方面由于破壞了PML核體的正常功能;另一方面即PML/RAR 癌蛋白本身的功能障礙。
在最新的這篇研究中,研究人員通過X射線晶體衍射技術(shù)成功解析了PML-B1 box結(jié)構(gòu)域的結(jié)構(gòu),并且首次提純到PML大片段,利用PML大片段首次在溶液觀察到PML核體的動(dòng)態(tài)組裝模式。并且通過對ATO的反應(yīng)進(jìn)一步探究了RING和B1-box聚合的先后順序,提出RING四聚體形成可能先于B1的寡聚化,即RING先形成四聚體進(jìn)而B1再形成更高程度的聚合,從而加深了對PML組裝機(jī)制的了解。
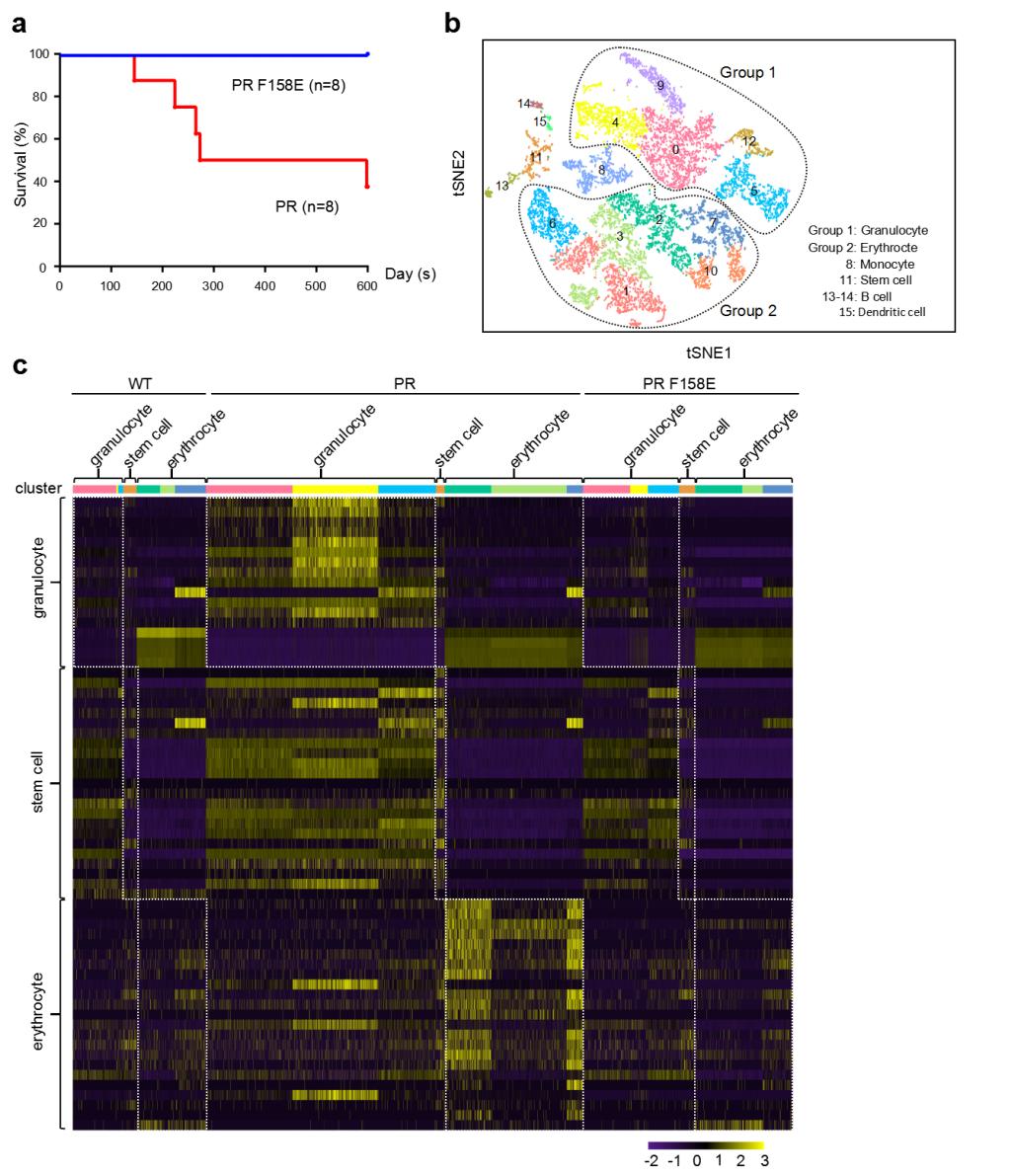
為了進(jìn)一步探究聚合與APL發(fā)生的關(guān)系,研究人員通過轉(zhuǎn)基因動(dòng)物實(shí)驗(yàn)及單細(xì)胞測序技術(shù)發(fā)現(xiàn),PML-B1 box的寡聚化對于APL的發(fā)病至關(guān)重要。并且通過單細(xì)胞RNA測序篩選到一大批聚合影響發(fā)病的新基因,并且其中的Trib3以及Atf5曾被報(bào)道在AML病人中高表達(dá)。這些新基因的發(fā)現(xiàn)為后續(xù)研究工作者探究聚合影響發(fā)病提供新的方向。更重要的是,該文首次提出了癌蛋白的寡聚可以作為靶向治療的新思路。蒙國宇教授為文章的通訊作者。博士生李玉文、馬曉丹、陳志明、武海燕和王鵬然為文章的共同第一作者。該研究獲得國家自然科學(xué)基金、上海市科委重點(diǎn)、教委高峰高原基金等項(xiàng)目以及上海同步輻射光源BL19U2、BL17U等線站的支持。
文章鏈接:https://www.nature.com/articles/s41467-019-11746-0

