6月24日,上海市免疫學(xué)研究所鄧劉福研究員團(tuán)隊(duì)在國(guó)際轉(zhuǎn)化醫(yī)學(xué)領(lǐng)域著名期刊《科學(xué)轉(zhuǎn)化醫(yī)學(xué)》(Science Translational Medicine)在線發(fā)表題為“cGAS-STING–mediated DNA sensing maintains CD8+T cell stemness and promotes antitumor T cell therapy”的研究論文。該研究揭示了內(nèi)源性cGAS-STING信號(hào)通過(guò)維持CD8+T細(xì)胞的“干性”促進(jìn)T細(xì)胞抗腫瘤免疫應(yīng)答的作用機(jī)制,為提高臨床T細(xì)胞治療效果提供了新的策略和依據(jù)。
免疫治療是當(dāng)前腫瘤治療領(lǐng)域的熱點(diǎn),基于T細(xì)胞的免疫治療在根除實(shí)體瘤方面遇到了多重挑戰(zhàn)。T細(xì)胞治療最大的優(yōu)勢(shì)在于可特異性識(shí)別腫瘤抗原,從而有效殺傷腫瘤細(xì)胞防止腫瘤免疫逃逸。但持續(xù)的抗原刺激會(huì)導(dǎo)致T細(xì)胞耗竭,表面抑制性受體(如PD-1等)增加及效應(yīng)功能下降。目前,可以通過(guò)阻斷PD-1通路重新激活耗竭CD8+T細(xì)胞應(yīng)答,讓“精疲力竭”的T細(xì)胞“滿血復(fù)活”,但該策略仍受到T細(xì)胞質(zhì)量的限制。因此如何改善T細(xì)胞的質(zhì)量使免疫治療的T細(xì)胞維持更長(zhǎng)的時(shí)間,促使它們復(fù)制和擴(kuò)增是提高T細(xì)胞治療效果的新策略。
此前,研究人員發(fā)現(xiàn)耗竭性T細(xì)胞具有干細(xì)胞樣細(xì)胞(Stem-cell like)和終末分化細(xì)胞(Terminal)兩個(gè)主要亞群。干細(xì)胞樣T細(xì)胞以自我更新、擴(kuò)增和多能性為特征,對(duì)于T細(xì)胞治療和免疫檢查點(diǎn)阻斷治療實(shí)現(xiàn)持久的抗腫瘤反應(yīng)至關(guān)重要。所以研究人員正在探索如何調(diào)節(jié)干細(xì)胞樣T細(xì)胞的產(chǎn)生和維持其“干細(xì)胞特性(stemness)”以達(dá)到優(yōu)化T細(xì)胞治療和免疫檢查點(diǎn)阻斷治療的目的。然而,內(nèi)源性非轉(zhuǎn)錄調(diào)節(jié)因子對(duì)T細(xì)胞“干性”的調(diào)節(jié)作用知之甚少。
cGAS(cyclic GMP–AMP synthase)-STING通路是啟動(dòng)抗腫瘤天然免疫應(yīng)答的重要途徑,有望成為使腫瘤由“冷”轉(zhuǎn)“熱”的新一代免疫治療靶點(diǎn)。該通路的作用機(jī)制為:cGAS感受DNA,產(chǎn)生第二信使cGAMP,進(jìn)而活化STING接頭蛋白形成二聚體,通過(guò)招募TBK1激活I(lǐng)RF3形成蛋白復(fù)合物來(lái)誘導(dǎo)IFN-β的產(chǎn)生。在腫瘤微環(huán)境中cGAS-STING通路已成為主導(dǎo)免疫檢查點(diǎn)阻斷、“do not eat me”信號(hào)阻斷、放療或PARP抑制劑治療等對(duì)細(xì)胞質(zhì)DNA作出反應(yīng)的主要途徑。目前cGAS-STING通路的研究主要集中于腫瘤細(xì)胞以及天然免疫細(xì)胞上,發(fā)現(xiàn)其在腫瘤免疫、細(xì)胞衰老、炎癥疾病以及病毒感染等過(guò)程中都發(fā)揮著非常重要的作用,但是對(duì)T細(xì)胞內(nèi)的cGAS-STING通路的變化了解甚少,尤其在腫瘤微環(huán)境中。

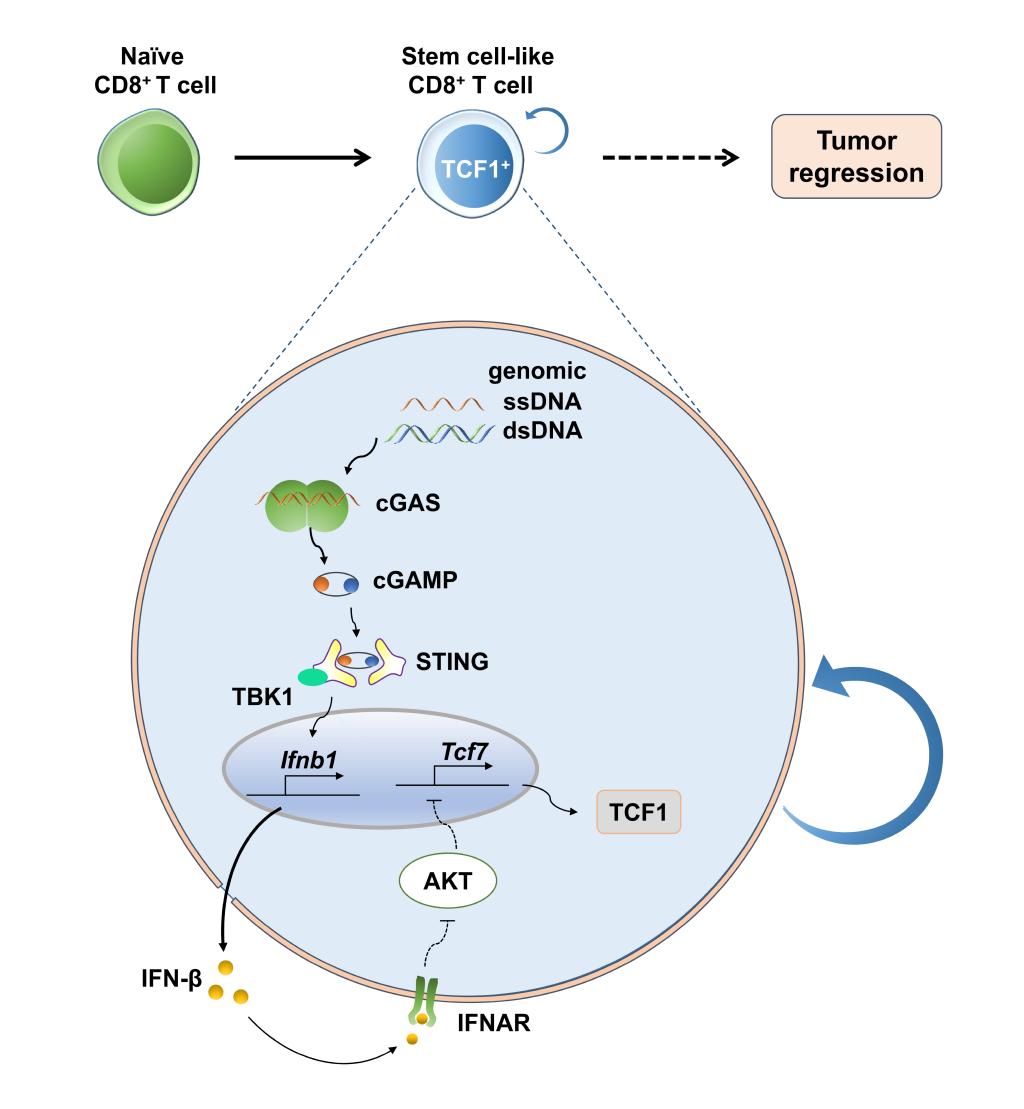
該研究發(fā)現(xiàn)在癌癥病人的外周血CD8+T細(xì)胞中cGAS和STING表達(dá)顯著下調(diào),提示cGAS和STING對(duì)于CD8+T細(xì)胞有著重要意義。應(yīng)用T細(xì)胞回輸治療小鼠腫瘤模型證明,CD8+T細(xì)胞內(nèi)cGAS和STING缺失會(huì)削弱T細(xì)胞治療腫瘤的效果。研究人員進(jìn)一步利用遺傳學(xué)、藥理學(xué)工具以及阻斷抗體來(lái)干擾cGAS-STING和I型干擾素信號(hào),證明該途徑對(duì)于維持抗腫瘤干細(xì)胞樣CD8+T細(xì)胞和最佳的抗腫瘤反應(yīng)是至關(guān)重要的。且發(fā)現(xiàn)cGAS和STING通過(guò)調(diào)節(jié)TCF1和Slamf6的表達(dá)影響腫瘤微環(huán)境中耗竭性CD8+T細(xì)胞的“干性”。cGAS-STING介導(dǎo)的I型干擾素信號(hào)以自分泌的形式增強(qiáng)干細(xì)胞樣CD8+T細(xì)胞的分化,同時(shí)通過(guò)抑制Akt的活性來(lái)阻止效應(yīng)因子的產(chǎn)生。此外,在體內(nèi)或體外的刺激下,基因組DNA在CD8+T細(xì)胞的胞漿中選擇性地富集,是T細(xì)胞中cGAS-STING通路活化的關(guān)鍵。人的外周血中也存在這樣一群細(xì)胞,既具有記憶細(xì)胞的特性,同時(shí)又具有干細(xì)胞的特征,命名為stem cell-like memory T cells(Tscm),這群細(xì)胞的增殖能力和抗腫瘤活性在所有T細(xì)胞亞群中是最強(qiáng)的。該研究發(fā)現(xiàn)STING激動(dòng)劑diABZI-C3可促進(jìn)健康志愿者和癌癥病人外周血中的Na?ve T細(xì)胞分化為Tscm亞群。更加令人振奮的是,進(jìn)一步應(yīng)用人源化小鼠模型發(fā)現(xiàn)STING激動(dòng)劑可以顯著提高CAR-T細(xì)胞治療A549實(shí)體瘤的效率。
該研究從免疫治療面臨的臨床問(wèn)題出發(fā),深入研究了CD8+T細(xì)胞內(nèi)源的cGAS-STING信號(hào)通路對(duì)T細(xì)胞的作用及機(jī)制;揭示了cGAS-STING通路通過(guò)維持CD8+T細(xì)胞的“干性”提高T細(xì)胞的治療效果;并在此基礎(chǔ)上,證明激活STING通路可以顯著提高人源CAR-T細(xì)胞治療實(shí)體瘤的效率。該研究揭示了內(nèi)源性cGAS-STING信號(hào)通過(guò)維持CD8+T細(xì)胞的“干性”促進(jìn)T細(xì)胞抗腫瘤免疫應(yīng)答的作用機(jī)制,為臨床治療過(guò)程中合理設(shè)計(jì)新型T細(xì)胞療法提供新的靶點(diǎn)。
最后,借用《西游記》中的孫悟空,來(lái)形象描繪該研究發(fā)現(xiàn)。西行取經(jīng)途中,為了降魔除妖(腫瘤細(xì)胞),孫悟空(CD8+T細(xì)胞)需要緊箍咒的法力(STING)和火眼金睛的魔力(cGAS),除卻雜念,克服萬(wàn)千艱難險(xiǎn)阻,獲得真經(jīng),修成正果。
該研究受到國(guó)家自然科學(xué)基金、國(guó)家海外青年高層次人才計(jì)劃、上海市科委和衛(wèi)健委的資助,該研究還得到上海市免疫學(xué)研究所公共平臺(tái)、上海交通大學(xué)基礎(chǔ)醫(yī)學(xué)院和仁濟(jì)醫(yī)院基礎(chǔ)-臨床創(chuàng)新研究中心研究平臺(tái)、上海市婦科腫瘤重點(diǎn)實(shí)驗(yàn)室的支持。論文的第一作者是助理研究員李文文與博士后路璐,通訊作者為上海交通大學(xué)醫(yī)學(xué)院上海市免疫學(xué)研究所鄧劉福研究員、上海交通大學(xué)附屬仁濟(jì)醫(yī)院狄文教授以及上海交通大學(xué)楊選明研究員。同時(shí),該研究還獲得了上海交通大學(xué)醫(yī)學(xué)院程金科教授和蘇冰教授、UT Southwestern Medical Center傅陽(yáng)心教授、同濟(jì)大學(xué)戈寶學(xué)教授和中科院生物物理研究所王盛典研究員的支持幫助。
文章鏈接:https://stm.sciencemag.org/content/12/549/eaay9013

