幽門螺桿菌(Helicobacter pylori,HP)是寄生于人類胃幽門部位的常見細菌病原體,,其長期感染易誘發(fā)慢性胃炎,、胃潰瘍甚至胃癌,是全球感染人數最多且潛在致癌危害最大的致病菌之一,。目前臨床上對HP的根除治療主要依賴多聯抗生素療法,,然而多聯抗生素的長期使用容易造成腸道菌群失調,引發(fā)其他病癥,,同時還導致了HP耐藥性逐步增強,,根除率逐年降低。因此,研究HP化學生物學調控新機制和發(fā)展抗HP新藥具有重要科學意義和轉化價值,。
上海交通大學醫(yī)學院張良研究員等課題組于11月26日在Nature Communications在線發(fā)表研究論文,,題目為“Helicobacter pyloriFabX contains a [4Fe-4S] cluster essential for unsaturated fatty acid synthesis”。該研究闡明了HP特有的脂肪酸脫氫異構酶FabX對飽和脂肪酰修飾ACP底物的選擇性識別和催化調控的化學生物學機制,,明確了HP不飽和脂肪酸合成與分泌ROS腐蝕胃黏膜病理功能之間的密切關聯,,為抗HP創(chuàng)新藥物研發(fā)提供了科學依據。
II型脂肪酸合成途徑(FAS-II)是細菌的主要基礎代謝途徑,,其酶系是公認的抗菌藥物靶標群,。底物載脂蛋白(Acyl Carrier Protein, ACP)為該途徑的核心,是脂肪酸底物的共價載體,。ACP通過其保守絲氨酸側鏈共價修飾脂肪酰底物,,并攜帶底物依次被該途徑中的七類酶識別并催化,從而完成對不飽和脂肪酸(Unsaturated Fatty Acid, UFA)和飽和脂肪酸(Saturated Fatty Acid, SFA)的合成,。由于存在ACP脂肪酰共價修飾難以在體外構建的技術瓶頸,,該途徑酶系識別和催化調控ACP-脂肪酰底物的化學生物學機制一直不甚明確,制約了該領域發(fā)展和相關藥物研發(fā),。

研究團隊首先發(fā)展了HP脂肪酸合成途徑底物載脂蛋白ACP與不同長度脂肪酰底物的體外共價修飾技術,,并證明FabX對長度為8碳和10碳的飽和脂肪酰底物具有選擇性脫氫催化活性。進一步解析了FabX,、FabX與磷脂酰泛酰修飾型ACP(holo-ACP),,以及FabX與8碳飽和脂肪酰修飾型ACP(8C-ACP)的復合物晶體結構。通過電子順磁共振技術(Electron paramagnanetic resonance, EPR)研究發(fā)現,,FabX利用位于活性中心FMN附近的氨基酸His182對飽和脂肪酰底物進行親核攻擊,,觸發(fā)脫氫催化反應。更重要的是,,FabX利用獨特的FMN和[4Fe-4S]鐵硫簇雙活性中心對脫氫產生的2對電子/質子進行往返傳遞和臨時儲存,,并在反應結束后將電子最終傳遞給穩(wěn)定在His182附近負氧離子洞中的氧氣分子,生成超氧分子,,揭示了這種FMN-[4Fe-4S]雙活性中心之間電子往返傳遞和存儲的獨特分子機制,。最后,HP通過將超氧分子快速排至胞外,,促進腐蝕胃黏膜的病理作用,,闡明了脂肪酸合成與HP病理作用之間的密切關聯。該工作在審稿期間被審稿人高度評價為“This is a great contribution to the field of bacterial fatty acid biosynthesis”,。
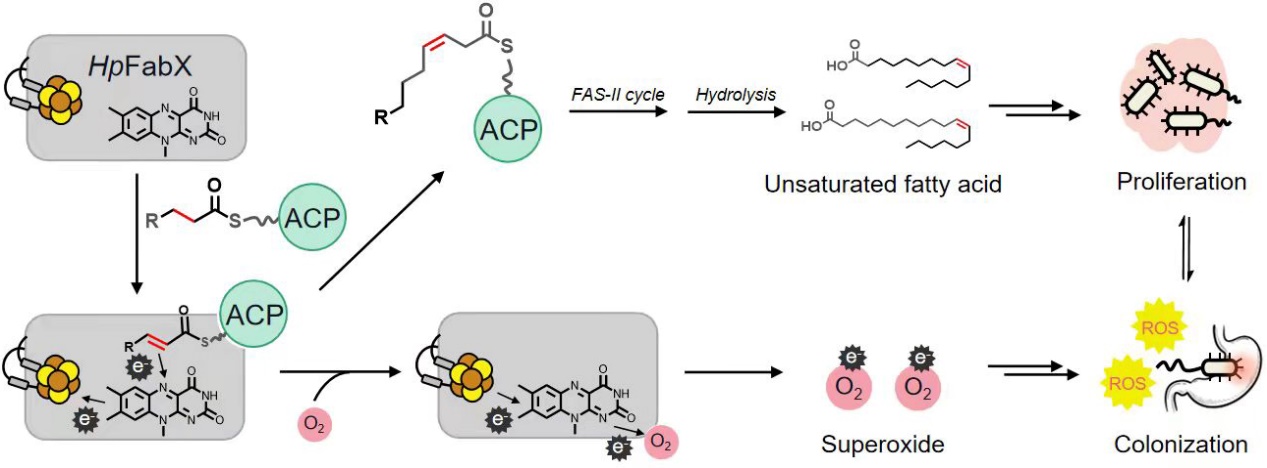
圖1 HP不飽和脂肪酸合成關鍵酶FabX的催化分子機制和功能
上海交通大學醫(yī)學院張良研究員、南京醫(yī)科大學畢洪凱教授,、美國伊利諾伊大學香檳分校John E. Cornan教授和上海中醫(yī)藥大學陳紅專教授為該論文的共同通訊作者,。上海交通大學醫(yī)學院2020級博士生周甲申、博士后張琳、南京醫(yī)科大學實驗師曾利平,、中科院合肥強磁場中心于璐副研究員,、南京醫(yī)科大學實驗師段園園和上海交通大學醫(yī)學院2016級碩士生沈思琪為該論文的共同第一作者。該工作受到了中國科學技術大學田長麟教授,、中國科學院深圳先進技術研究院合成所周佳海研究員,、復旦大學藥學院周璐教授、南京中醫(yī)藥大學張毅楠教授和上海交通大學醫(yī)學院附屬仁濟醫(yī)院林厚文教授的指導和大力支持,,并受到了國家基金委重大研發(fā)計劃和面上項目,、上海市科委和教委等項目的資助。

