基礎(chǔ)醫(yī)學(xué)院生物化學(xué)與分子細(xì)胞生物學(xué)系的賈浩副研究員等最近在Molecular Therapy雜志上發(fā)表了題為“LncRNA IFITM4P is activated through LPS/TLR4 and promotes immune escape by up-regulating PD-L1 via dual mechanism during oral carcinogenesis”的學(xué)術(shù)文章。
口腔白斑病(oral leukoplakia)是最重要的口腔黏膜潛在惡性疾患之一,上皮異常增生是其病理學(xué)特征。世界衛(wèi)生組織將口腔黏膜癌前病變和癌前狀態(tài)歸為口腔黏膜潛在惡性疾患,口腔白斑病從單純上皮異常增生、輕-中-重度上皮異常增生到惡變的各階段較明確,而且口腔部位相對(duì)表淺易于觀測(cè),可作為全身癌前病變的代表疾病,是癌前病變發(fā)生發(fā)展的良好研究模型。目前,藥物的局部、全身治療與手術(shù)、激光、冷凍、光動(dòng)力等療法均不能有效降低口腔白斑病的癌變率,并且口腔白斑病還存在易復(fù)發(fā)、多發(fā)、多次癌變等臨床困境。因此,針對(duì)口腔白斑白斑病研發(fā)具有抑制和逆轉(zhuǎn)作用的全身用藥,特別是對(duì)于口腔黏膜具有區(qū)域化癌變潛能的患者,具有重要的臨床意義和社會(huì)價(jià)值。
研究人員利用口腔黏膜白斑病組織和口腔鱗癌組織樣本通過(guò)高通量篩選的方法,分析發(fā)現(xiàn)了PD-L1的表達(dá)水平隨著組織惡性程度的增加而升高。局部炎癥明顯的口腔黏膜白斑病患者的惡性進(jìn)展更快。在實(shí)驗(yàn)中首次構(gòu)建了LPS(脂多糖)聯(lián)合4NQO誘導(dǎo)的【炎癥-口腔白斑小鼠模型】進(jìn)行治療研究,通過(guò)給患病小鼠注射PD-1抗體后,發(fā)現(xiàn)PD-1抗體可以顯著阻斷口腔白斑惡性進(jìn)展,令人驚喜的是,PD-1抗體對(duì)炎癥誘發(fā)的小鼠白斑惡性進(jìn)展模型具有更好的抑制效果。
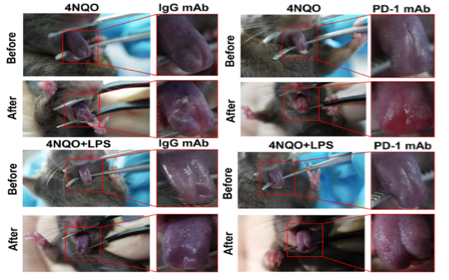
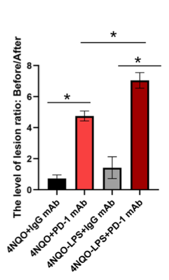
團(tuán)隊(duì)研究人員進(jìn)一步利用基因高通量篩選發(fā)現(xiàn):相較于正常組織,在人的口腔黏膜白斑病/鱗癌組織中長(zhǎng)鏈非編碼RNA IFITM4P高表達(dá),其表達(dá)水平隨著惡性程度的增加而升高。研究還發(fā)現(xiàn)了非編碼RNA IFITM4P受LPS刺激后,可以進(jìn)行核質(zhì)穿梭,具體的原因還不清楚。在細(xì)胞質(zhì)內(nèi),IFITM4P與SASH1形成復(fù)合體,通過(guò)磷酸化激活了TAK1-NF-κB途徑,NF-κB的入核促進(jìn)了PD-L1的表達(dá)。LPS的處理可以促進(jìn)IFITM4P的入核,進(jìn)一步通過(guò)招募去甲基化酶KDM5A結(jié)合并抑制了PTEN的表達(dá),進(jìn)而削弱了PTEN對(duì)PD-L1的抑制作用,上調(diào)了PD-L1的表達(dá)。IFITM4P通過(guò)胞質(zhì)和胞核兩種機(jī)制協(xié)同促進(jìn)了口腔白斑/鱗癌細(xì)胞中PD-L1的表達(dá),促使口腔黏膜白斑病發(fā)生免疫逃逸。因此,IFITM4P可作為早期診斷口腔黏膜白斑病惡變的指標(biāo)。同時(shí)團(tuán)隊(duì)研究人員利用動(dòng)物模型也發(fā)現(xiàn)了IFITM4P高表達(dá)的荷瘤小鼠對(duì)PD-1單抗的響應(yīng)更好,可考慮將PD-1抗體作為治療高表達(dá)IFITM4P口腔黏膜白斑病的有效治療方式。

附屬第九人民醫(yī)院口腔黏膜病科副主任醫(yī)生施琳俊,基礎(chǔ)醫(yī)學(xué)院生化細(xì)胞系碩士生楊于權(quán),博士生李夢(mèng)瑩為該論文的共同第一作者;基礎(chǔ)醫(yī)學(xué)院的賈浩副研究員,侯照遠(yuǎn)研究員及附屬第九人民醫(yī)院口腔黏膜病科沈雪敏主任醫(yī)師為該論文的共同通訊作者。該研究工作還得到了國(guó)家自然科學(xué)基金、上海市科技啟明星,上海市科委等經(jīng)費(fèi)的資助。

