6月14日,上海交通大學(xué)醫(yī)學(xué)院上海市免疫學(xué)研究所吳學(xué)鋒課題組等在國(guó)際學(xué)術(shù)期刊Cell Reports在線發(fā)表題為“Vps33B controls Treg cell suppressive function through inhibiting lysosomal nutrient sensing complex-mediated mTORC1 activation”的研究論文,研究揭示了囊泡蛋白33B(Vps33B)在通過(guò)維持內(nèi)體/溶酶體系統(tǒng)穩(wěn)態(tài)來(lái)調(diào)控氨基酸信號(hào)依賴的mTORC1通路的激活和細(xì)胞代謝,從而維持調(diào)節(jié)性T細(xì)胞的抑制功能。

調(diào)節(jié)性T(Treg)細(xì)胞在維持免疫穩(wěn)態(tài)和控制免疫耐受中不可或缺。但Treg細(xì)胞的免疫抑制作用,既能防御人體發(fā)生自身免疫性疾病,又能抑制抗腫瘤免疫促使腫瘤細(xì)胞發(fā)生免疫逃逸,間接促進(jìn)腫瘤細(xì)胞的增殖。因此在抗腫瘤免疫中,如何降低Treg細(xì)胞的抑制功能非常關(guān)鍵。Treg細(xì)胞的抑制功能受到mTORC1通路的嚴(yán)密調(diào)控,mTOR通路的抑制或過(guò)度激活均影響Treg細(xì)胞的穩(wěn)定性和功能。Treg細(xì)胞中mTORC1的過(guò)度激活會(huì)促使糖酵解水平升高,這會(huì)導(dǎo)致Treg標(biāo)志性分子Foxp3水平降低,增強(qiáng)Treg細(xì)胞的不穩(wěn)定性并使其向效應(yīng)T細(xì)胞轉(zhuǎn)化,致使炎癥條件下Treg細(xì)胞抑制功能的喪失,然而mTORC1激活的動(dòng)態(tài)和負(fù)調(diào)控機(jī)制仍不清楚。真核細(xì)胞中高度有序的內(nèi)溶酶體系統(tǒng)對(duì)于細(xì)胞營(yíng)養(yǎng)感應(yīng)至關(guān)重要。近年來(lái)多項(xiàng)研究表明Vps33B介導(dǎo)內(nèi)體/溶酶體系統(tǒng)中的囊泡運(yùn)輸以及外泌體分泌,由此對(duì)肝臟、造血、腫瘤的發(fā)生發(fā)展產(chǎn)生影響,但該蛋白及其所調(diào)控的內(nèi)體/溶酶體系統(tǒng)如何控制Treg細(xì)胞的穩(wěn)態(tài)和功能仍未知。
本項(xiàng)研究表明,Vps33B特異性缺失導(dǎo)致Treg細(xì)胞抑制功能缺陷并出現(xiàn)效應(yīng)型T細(xì)胞表型,Treg抑制功能缺乏會(huì)導(dǎo)致小鼠T細(xì)胞穩(wěn)態(tài)紊亂和T細(xì)胞效應(yīng)性增強(qiáng),從而使小鼠抗腫瘤免疫增強(qiáng)。機(jī)制方面,Vps33B與位于晚期內(nèi)體/溶酶體上的mTORC1招募、激活必備元件——溶酶體營(yíng)養(yǎng)感應(yīng)復(fù)合物(LYNUS)結(jié)合,促進(jìn)晚期內(nèi)體和溶酶體融合,清除含有LYNUS的晚期內(nèi)體/溶酶體,從而抑制mTORC1的激活。Treg細(xì)胞中Vps33B的缺失導(dǎo)致內(nèi)體溶酶體融合受阻,進(jìn)而導(dǎo)致LYNUS積累,使得mTORC1過(guò)度激活、糖酵解代謝水平上調(diào)、Foxp3表達(dá)水平和免疫抑制功能下降。綜上所述,Vps33B通過(guò)維持內(nèi)體/溶酶體穩(wěn)態(tài)來(lái)調(diào)控氨基酸信號(hào)依賴的mTORC1的激活和細(xì)胞代謝,從而維持Treg細(xì)胞的抑制功能。該研究揭示靶向Treg細(xì)胞中的Vps33B是臨床上提高抗腫瘤免疫力的潛在治療策略。
上海市免疫學(xué)研究所2017級(jí)直博生項(xiàng)鴻睿是本研究論文的第一作者,通訊作者為上海市免疫學(xué)研究所的吳學(xué)鋒研究員、鄒強(qiáng)研究員和上海交通大學(xué)基礎(chǔ)醫(yī)學(xué)院劉俊嶺研究員。本研究得到國(guó)家重點(diǎn)研發(fā)計(jì)劃干細(xì)胞及轉(zhuǎn)化專項(xiàng)、國(guó)家自然科學(xué)基金、上海市科委項(xiàng)目、細(xì)胞分化與凋亡教育部重點(diǎn)實(shí)驗(yàn)室和上海市細(xì)胞穩(wěn)態(tài)調(diào)控與疾病前沿科學(xué)研究基地等的支持,上海市免疫學(xué)研究所及上海交通大學(xué)醫(yī)學(xué)院基礎(chǔ)醫(yī)學(xué)院公共技術(shù)平臺(tái)和動(dòng)物科學(xué)部提供支持。上海交通大學(xué)醫(yī)學(xué)院附屬瑞金醫(yī)院王正廷副主任醫(yī)師、上海交通大學(xué)基礎(chǔ)醫(yī)學(xué)院鐘清研究員、上海市免疫學(xué)研究所葉幼瓊研究員、陳磊研究員及課題組成員等提供幫助。
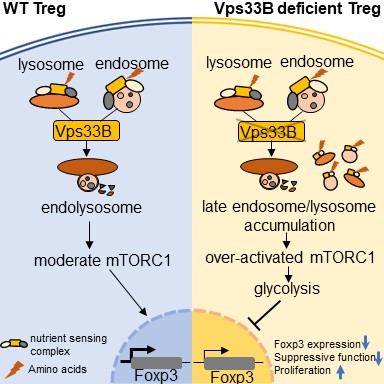
研究模型圖:Vps33B缺失導(dǎo)致Treg細(xì)胞內(nèi)體溶酶體融合受阻,進(jìn)而促使溶酶體營(yíng)養(yǎng)感應(yīng)復(fù)合物(LYNUS)積累,mTORC1過(guò)度激活、糖酵解代謝水平上調(diào)、Foxp3表達(dá)和免疫抑制功能下降。
課題組簡(jiǎn)介:課題組長(zhǎng)吳學(xué)鋒,入選國(guó)家高層次人才計(jì)劃青年項(xiàng)目。南開大學(xué)學(xué)士、碩士、美國(guó)賓州州立大學(xué)免疫學(xué)博士。美國(guó)德克薩斯大學(xué)M.D.安德森癌癥中心、加州大學(xué)圣地亞哥分校博士后。加入上海交通大學(xué)醫(yī)學(xué)院上海市免疫學(xué)研究所前在美國(guó)知名制藥公司擔(dān)任Senior Scientist,從事癌癥免疫藥物開發(fā)研究。課題組以開發(fā)治療免疫疾病和癌癥的藥物和新策略為目標(biāo),聚焦連接炎癥和腫瘤的細(xì)胞和分子機(jī)制,開展以下研究:1.研究巨噬細(xì)胞和樹突狀細(xì)胞免疫代謝調(diào)控機(jī)制(European Journal of Immunology, 2022;Journal of Immunology, 2021;Theranostics, 2021);2.探討應(yīng)激反應(yīng)對(duì)T細(xì)胞和調(diào)節(jié)性T細(xì)胞代謝穩(wěn)態(tài)和抗腫瘤免疫力的調(diào)控(Cell Reports, 2022;Nature Communications, 2021);3.闡述腫瘤細(xì)胞來(lái)源的信號(hào)如何調(diào)控其微環(huán)境中的免疫細(xì)胞和免疫反應(yīng)以探究腫瘤轉(zhuǎn)移機(jī)制。課題組得到國(guó)家重點(diǎn)研發(fā)計(jì)劃、國(guó)家自然科學(xué)基金、上海市科委項(xiàng)目等的經(jīng)費(fèi)支持,面向海內(nèi)外招聘博士后,將提供上海地區(qū)具有競(jìng)爭(zhēng)力的待遇、一流的研究平臺(tái)和良好的發(fā)展前景。熱忱歡迎青年才俊聯(lián)系加入課題組。(實(shí)驗(yàn)室網(wǎng)頁(yè):http://dripwizz.com/sii/info/1053/2087.htm;電子郵箱:[email protected])。

