生物醫(yī)學成像在癌癥診斷、術(shù)中指導和術(shù)后評估中起著非常重要的作用。熒光成像由于其低成本、快速反饋、高靈敏度、非危險輻射等特點,在生物醫(yī)學研究中引起了廣泛的關(guān)注。
常規(guī)光學成像中使用的激發(fā)光通常是可見光,由于存在組織吸收和光散射,激發(fā)光在穿透生物組織時會大大衰減。而使用近紅外(650~900nm)激發(fā)光可以實現(xiàn)更深的組織穿透以及更低的組織自發(fā)熒光,從而得到高信號背景比(signal-to-background ratio, SBR)的深層組織成像。
FDA于2021年已批準Cytalux(pafolacianine sodium;既往稱為OTL38)用于成年卵巢癌患者,作為術(shù)中識別惡性病變的輔助手段。Cytalux作為一種近紅外診斷試劑,術(shù)前以靜脈注射的形式給藥。由于卵巢癌通常會導致細胞膜的葉酸受體高表達,Cytalux進入人體后會與葉酸受體特異性結(jié)合并在近紅外照射下發(fā)光,從而幫助外科醫(yī)生精準定位并切除癌變組織。由此,靶向腫瘤的近紅外熒光造影劑已經(jīng)成為未來新藥研發(fā)領(lǐng)域的新興熱點。

近日,上海交通大學醫(yī)學院鐘清、王偉衛(wèi)課題組,聯(lián)合上海交通大學醫(yī)學院附屬第九人民醫(yī)院的徐斌、陳其課題組,以及上海交通大學醫(yī)學院附屬瑞金醫(yī)院的陳露課題組,在Life Medicine發(fā)表了題為“A Novel Spraying Nanoprobe for Renal Cell Carcinoma in Humans”的文章。文章報道了一種簡單、高效且設計優(yōu)良的腫瘤組織成像方法,只需將合成的納米顆粒水溶液直接噴涂到腫瘤組織的表面,即可實現(xiàn)術(shù)中實時腫瘤成像。
該文報道了用近紅外低氧靶向染料(Dye)和陰離子表面活性劑(Surfactin)自組裝而成的納米顆粒S-4-NP。S-4-NP因其納米結(jié)構(gòu)的存在,在細胞外為自淬滅狀態(tài)。當S-4-NP與腫瘤細胞接觸后,Dye可以特異地識別出在細胞膜上的有機陰離子轉(zhuǎn)運多肽(Organic anion-transporting polypeptides, OATPs),然后從納米粒子中釋放到細胞內(nèi)。在細胞中,游離的Dye會被活化,能夠被近紅外光激發(fā),從而對腫瘤細胞進行標記(圖1)。
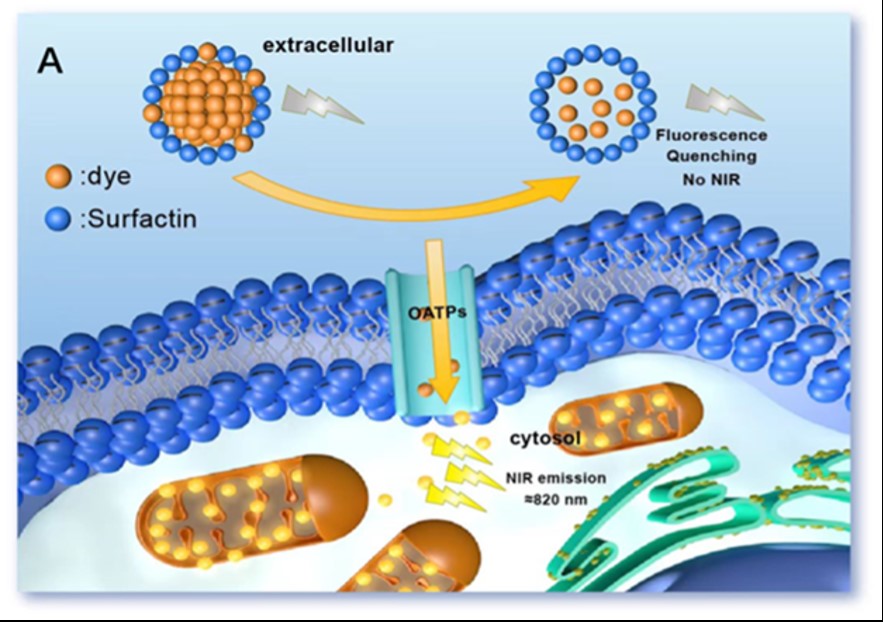
圖1 小鼠成瘤模型驗證
從荷瘤小鼠取出腫瘤后,立即將S-4-NP溶液噴涂于腫瘤組織上。在噴涂后3min、6min、9min和12min對樣品進行近紅外成像。近紅外信號的強度在3~12min內(nèi)也有顯著提高(>2倍),表明其穩(wěn)定性好。
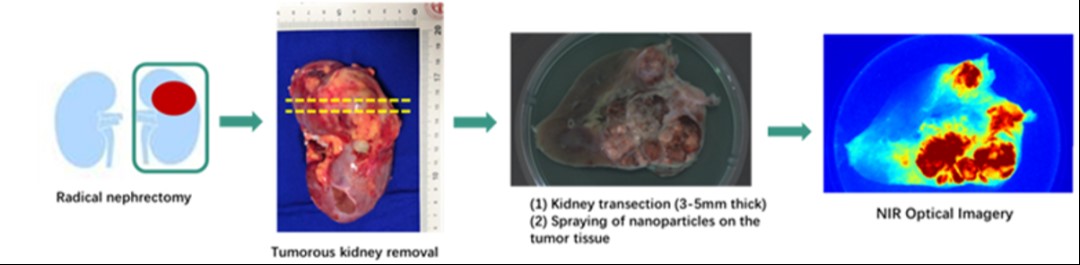
圖2 根治性腎切除術(shù)驗證
本文重點研究了S-4-NP在臨床腎癌切除手術(shù)中的應用(圖2)。
保留腎單位手術(shù)(Nephron-sparing surgery, NSS)是早期腎癌(Renal cell carcinoma, RCC)治療中最主要的一種方法,旨在根治腫瘤的同時,最大限度保留腎臟功能。但保留腎單位手術(shù)后手術(shù)切緣陽性(Positive surgical margins, PSMs)仍然無法徹底避免,并且與局部復發(fā)、生存率降低相關(guān)。目前臨床上仍缺乏快速響應的、無毒的腫瘤特異性造影劑探測切緣。
在手術(shù)中,S-4-NP可以直接噴灑與離體的腫瘤組織切面,通過近紅外成像可以在3分鐘內(nèi)清晰的標識腫瘤組織,從而幫助臨床手術(shù)醫(yī)生快速區(qū)分腫瘤組織與正常組織的邊界,對手術(shù)切緣進行判斷(完整成像視頻見圖3)。
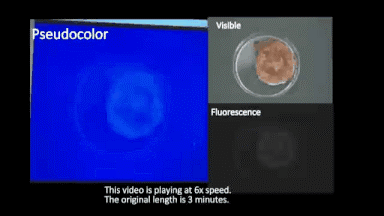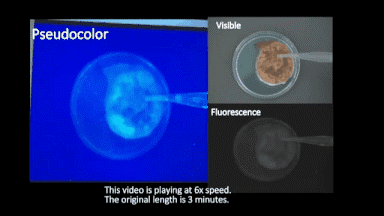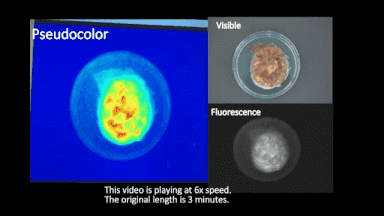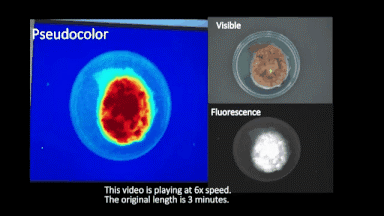
圖3
保留腎單位手術(shù)是治療早期腎腫瘤的首選手術(shù)技術(shù)。但切緣陽性的問題仍然值得關(guān)注,過去通常依靠術(shù)中外科醫(yī)生肉眼判斷腫瘤切緣。對懷疑部位的確認,需要等待較長時間的冰凍切片或最終的石蠟切片。該成像方法快速、高效,使得外科醫(yī)生在發(fā)現(xiàn)切緣陽性后可以馬上采取補救措施,可以有效縮短手術(shù)時間,改善病人預后,降低腫瘤復發(fā)率,具有重要的臨床轉(zhuǎn)化意義。

