全球每年有約有5000萬(wàn)例膿毒癥患者,其中死亡人數(shù)超20%,每年死于膿毒癥的患者約占全球死亡人數(shù)的1/5。膿毒癥病因復(fù)雜,主要是由于感染造成的凝血系統(tǒng)和免疫系統(tǒng)功能紊亂,進(jìn)而導(dǎo)致彌散性血管內(nèi)凝血、微血栓形成、急性肺損傷以及多器官衰竭。血小板數(shù)目減少和功能障礙是臨床上判斷膿毒癥嚴(yán)重程度和預(yù)后的重要指標(biāo)。血小板是由巨核細(xì)胞分化形成的無(wú)核血細(xì)胞,除了傳統(tǒng)的凝止血功能外,也具有免疫調(diào)控功能。活化的血小板可通過(guò)釋放血小板衍生的微泡(PMVS)、細(xì)胞因子(IL-1β和TGF-β等)和趨化因子(CXCL4和CXCL7等),直接參與天然免疫的調(diào)控。此外,血小板表面的P-selectin也可和中性粒細(xì)胞表面的PSGL1結(jié)合,從而調(diào)控感染時(shí)中性粒細(xì)胞的NETosis過(guò)程,影響其對(duì)病原體的捕獲和殺傷能力。過(guò)度活化的血小板卻是膿毒癥血栓的形成的重要病理基礎(chǔ),在膿毒癥進(jìn)程中是一把“雙刃劍”。然而,在膿毒癥中,血小板如何識(shí)別病原體相關(guān)分子模式(PAMPs),并介導(dǎo)其活化過(guò)程卻仍然缺乏研究。

3月20日,上海交通大學(xué)醫(yī)學(xué)院劉俊嶺教授團(tuán)隊(duì)徐艷艷副研究員等在Immunity雜志在線發(fā)表名為“STING activation in platelets aggravates septic thrombosis by enhancing platelet activation and granule secretion”的文章。系統(tǒng)地揭示了血小板如何響應(yīng)細(xì)菌等微生物感染刺激并引起血小板顆粒釋放的深層機(jī)制。該研究中,研究者們利用活體成像技術(shù),發(fā)現(xiàn)血小板STING缺失可減輕膿毒癥誘發(fā)的小鼠肝臟和肺部微血栓和NETs結(jié)構(gòu)的形成,降低肝肺損傷和凝血異常相關(guān)指標(biāo),增強(qiáng)小鼠的生存率。體外實(shí)驗(yàn)方面,作者發(fā)現(xiàn)STING激動(dòng)劑cGAMP可增強(qiáng)血小板對(duì)如thrombin和collagen等刺激劑的響應(yīng)程度。然而,血小板作為一類(lèi)無(wú)核細(xì)胞,缺乏轉(zhuǎn)錄過(guò)程,作者發(fā)現(xiàn)cGAMP無(wú)法打開(kāi)血小板中STING/TBK1/IRF3信號(hào),卻可以促進(jìn)血小板STING的棕櫚酰化,提示血小板內(nèi)存在一條不同于STING/TBK1/IRF3的新型STING下游激活信號(hào)。
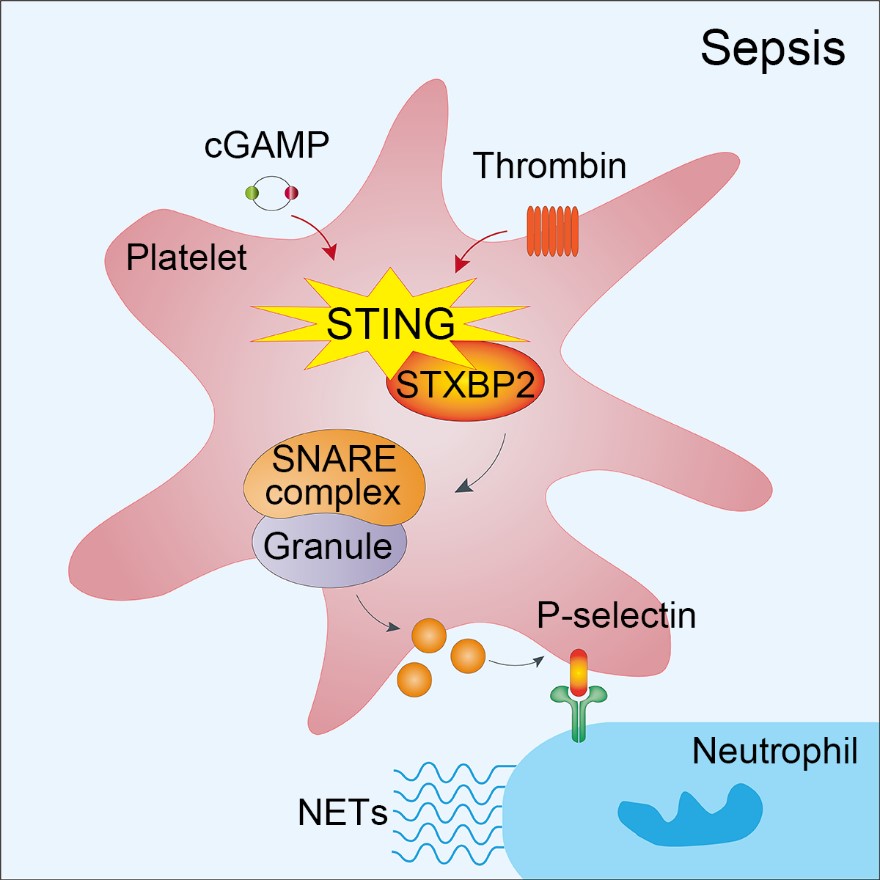
血小板內(nèi)部顆粒來(lái)源于巨核細(xì)胞的分界膜系統(tǒng)(DMS系統(tǒng)),儲(chǔ)存有大量免疫相關(guān)細(xì)胞因子與趨化因子。血小板顆粒分泌依賴(lài)于SNARE復(fù)合物的裝配,作者發(fā)現(xiàn)血小板STING可與分泌相關(guān)蛋白STXBP2結(jié)合,維持SNARE復(fù)合物的有效裝配;而cGAMP引起的血小板STING棕櫚酰化則會(huì)進(jìn)一步促進(jìn)SNARE復(fù)合物的裝配,導(dǎo)致感染過(guò)程中血小板顆粒過(guò)度分泌。作者進(jìn)而通過(guò)“Protein-Protein Docking”手段,發(fā)現(xiàn)了STING與STXBP2的潛在結(jié)合區(qū)域,并對(duì)此設(shè)計(jì)了相應(yīng)多肽,發(fā)現(xiàn)該肽段能靶向二者結(jié)合,并減弱血小板活化和感染誘導(dǎo)的微血栓形成。
綜上,該研究發(fā)現(xiàn)了血小板STING活化的獨(dú)特作用,揭示了血小板STING調(diào)控膿毒癥感染的作用機(jī)制,為膿毒癥提供了新的治療策略。此外,該工作也提示,針對(duì)靶向激活STING的抗腫瘤免疫治療策略可能存在潛在的致栓風(fēng)險(xiǎn),需引起警示。
劉俊嶺教授團(tuán)隊(duì)博士研究生楊咪娜和姜豪杰博士后為論文的共同第一作者,徐艷艷副研究員、劉俊嶺教授和姜豪杰博士后為該論文共同通訊作者。該研究得到了國(guó)家重點(diǎn)研發(fā)計(jì)劃,國(guó)家自然科學(xué)基金重點(diǎn)項(xiàng)目、面上項(xiàng)目等多項(xiàng)資金的大力資助。

