兒童急性淋巴細胞白血病(acute lymphoblastic leukemia, ALL)是兒童時期最常見的癌癥類型,在兒童白血病中占比超過80%。國家兒童醫(yī)學中心(上海)、附屬上海兒童醫(yī)學中心牽頭的中國抗癌協(xié)會小兒腫瘤專委會急性淋巴細胞白血病(CCCG-ALL-2015)多中心協(xié)作組持續(xù)優(yōu)化現(xiàn)有臨床治療方案,使得中國兒童的ALL預后顯著提升,接近國際先進水準。但耐藥復發(fā)、難治ALL治療策略有限等問題仍然是近年來兒童白血病領域的研究熱點和難點,也是約束我國兒童ALL治愈率進一步提高的瓶頸。

近期,附屬上海兒童醫(yī)學中心周斌兵課題組在Leukemia期刊上發(fā)表了最新研究成果“Targeting DNA polymerase β elicits synthetic lethality with mismatch repair deficiency in acute lymphoblastic leukemia (靶向DNA聚合酶β在錯配修復缺陷型急性淋巴細胞白血病中引起合成致死效應)”。該研究聚焦DNA重要修復通路之堿基切除修復(base excision repair, BER),探究其在ALL細胞耐藥存活中的作用,揭示了其在巰嘌呤引起的基因組損傷修復中所發(fā)揮的重要作用,并提出了POLB抑制劑聯(lián)合巰嘌呤用于ALL治療的潛在策略。
本研究通過對兒童ALL患者的全基因組測序發(fā)現(xiàn),MMR通路核心基因(例如MSH2, MSH6和PMS2)突變是導致巰嘌呤耐藥的重要原因之一,在藥物壓力下促進“高突變”(hypermutation)和復發(fā)特異性突變印跡(thio-dMMR signature)的產(chǎn)生,誘導了耐藥突變的產(chǎn)生,進而導致ALL復發(fā)。目前研究認為,耐藥突變的產(chǎn)生與DNA損傷錯誤修復有關,但是對MMR缺失時巰嘌呤誘導的DNA損傷修復機制仍認識有限。
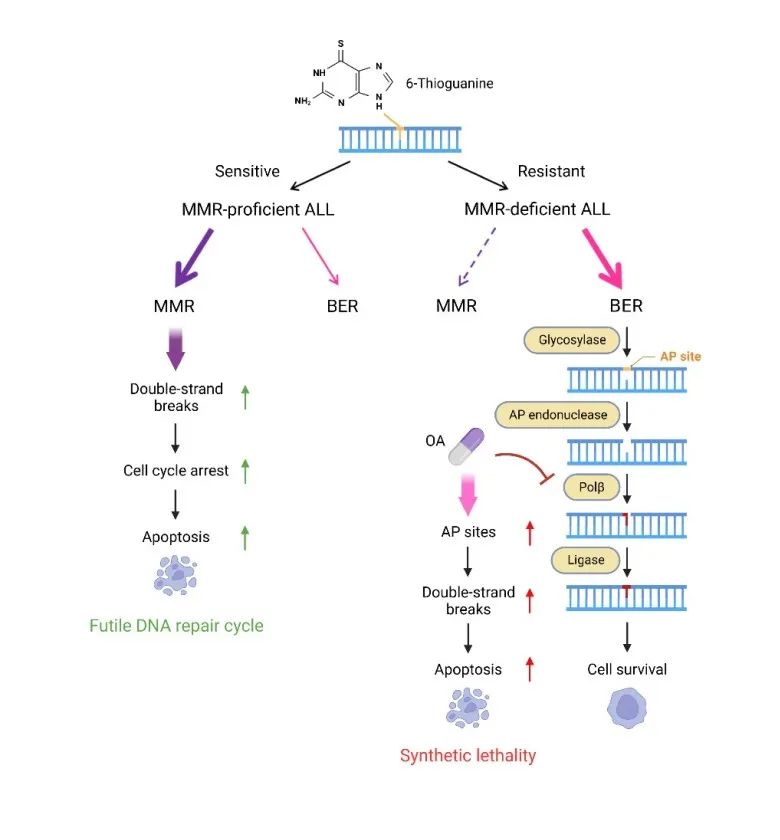
本研究發(fā)現(xiàn),BER通路關鍵聚合酶POLB在介導MMR缺陷的ALL細胞對巰嘌呤耐藥和存活中發(fā)揮著重要作用。首先,在MMR功能分別正常和缺陷的ALL細胞模型中,分別敲除多種參與BER通路的修復因子,觀察到POLB缺失增加了MMR缺陷的耐藥細胞對巰嘌呤的藥物敏感性,提示BER和POLB作為潛在治療靶點的可能性。之后,研究團隊在MMR缺陷的ALL細胞模型中敲除POLB基因或使用POLB抑制劑處理,引起胞內無堿基(apurinic/apyrimidinic, AP)位點數(shù)量的增加,促進DNA單/雙鏈斷裂的積累,誘導細胞凋亡,表現(xiàn)出合成致死(synthetic lethality, SL)效應;同時發(fā)現(xiàn)POLB抑制劑與6-TG聯(lián)合使用時對MMR缺陷細胞表現(xiàn)出明顯的協(xié)同效應(synergistic effect),并分別在ALL細胞系、病人來源(patient-derived)的原代細胞和異種移植小鼠模型多個層面驗證了POLB抑制劑聯(lián)合6-TG在復發(fā)難治型ALL中的治療潛力。
本研究揭示了BER通路的DNA聚合酶POLB在巰嘌呤誘導的DNA損傷修復中的關鍵作用,提出了POLB作為MMR缺陷型ALL的潛在治療靶點的可行性,為進一步優(yōu)化兒童ALL巰嘌呤臨床精準用藥方案奠定了理論基礎。研究指出,若要提高該治療策略的臨床應用價值,亟需開發(fā)一系列具備強效性和特異性的POLB小分子抑制劑。相關研究工作在一定程度上提示,抑制BER通路的PAPR也可能產(chǎn)生類似的效果。

