脂滴作為細(xì)胞內(nèi)脂質(zhì)儲(chǔ)存細(xì)胞器,參與維持細(xì)胞內(nèi)脂質(zhì)穩(wěn)態(tài),具有動(dòng)態(tài)響應(yīng)能量代謝需求的功能,其功能障礙與多種代謝疾病密切相關(guān),如非酒精性脂肪性肝病、糖尿病、肥胖等。脂滴是高度動(dòng)態(tài)的細(xì)胞器,在生成與成熟過(guò)程中可通過(guò)三種途徑進(jìn)行擴(kuò)張:(1)脂滴融合;(2)從內(nèi)質(zhì)網(wǎng)轉(zhuǎn)運(yùn)中性脂;(3)脂滴表面中性脂質(zhì)原位合成。近年來(lái),針對(duì)脂滴生長(zhǎng)調(diào)控的研究越來(lái)越多,但脂滴融合的分子機(jī)制仍然不清楚。
SNAREs(可溶性N-乙基馬來(lái)酰亞胺敏感因子附著蛋白受體)是一類(lèi)具有SNARE結(jié)構(gòu)域的家族蛋白。組成SNARE復(fù)合物的SNAREs蛋白錨定在相鄰的膜結(jié)構(gòu)上,它們的SNARE結(jié)構(gòu)域能夠自發(fā)從N端到C端拉鏈?zhǔn)浇M裝成四束螺旋體,引發(fā)膜融合。SNAREs已經(jīng)被證明參與多種物種的不同膜性細(xì)胞器的融合過(guò)程,比如Vam3-Vti1-Vam7-Nyv1介導(dǎo)了酵母的液泡同型融合,STX1-SNAP25-VAMP2介導(dǎo)了哺乳動(dòng)物神經(jīng)遞質(zhì)釋放過(guò)程中突觸小泡與質(zhì)膜的融合,STX17-SNAP29-VAMP8以及YKT6-SNAP29-STX7驅(qū)動(dòng)了細(xì)胞自噬過(guò)程中自噬體與溶酶體的融合。但對(duì)于SNARE復(fù)合物是否也介導(dǎo)了脂滴融合過(guò)程一直未有定論。

11月21日,上海交通大學(xué)醫(yī)學(xué)院病理生理學(xué)系鐘清、留筱廈課題組與華中科技大學(xué)丁彬彬課題組在Cell Discovery在線發(fā)表題為Qa-SNARE syntaxin 18 mediates lipid droplet fusion with SNAP23 and SEC22B的合作研究論文,發(fā)現(xiàn)SNARE蛋白STX18、SNAP23、SEC22B可組裝成SNARE復(fù)合物,調(diào)控脂滴動(dòng)態(tài),并進(jìn)一步建立了全新的體外脂滴融合體系,直接證明了SNARE復(fù)合物介導(dǎo)脂滴融合的分子機(jī)制。
為了鑒定調(diào)控脂滴融合的SNAREs,研究團(tuán)隊(duì)利用siRNA篩選并結(jié)合蛋白質(zhì)組學(xué),發(fā)現(xiàn)Qa SNARE STX18、Qbc SNARE SNAP23、R SNARE SEC22B的缺失影響細(xì)胞內(nèi)脂滴的大小,但并不影響脂質(zhì)的生成、脂肪酸的攝取、脂解。此外,這三個(gè)SNAREs蛋白存在形成一套完整的SNARE復(fù)合物的可能性。因此,研究團(tuán)隊(duì)猜測(cè)細(xì)胞內(nèi)存在STX18-SNAP23-SEC22B復(fù)合物,可參與調(diào)控脂滴融合。接著,研究團(tuán)隊(duì)利用內(nèi)源性co-IP技術(shù)和一系列體外生化手段證明了這三個(gè)SNARE蛋白之間存在相互作用,可在體外組裝形成穩(wěn)定的SNARE復(fù)合物。利用共聚焦顯微鏡以及免疫金電鏡技術(shù),研究團(tuán)隊(duì)確認(rèn)了SNAREs在脂滴表面的定位,并且首次建立脂滴蛋白半胱氨酸標(biāo)記實(shí)驗(yàn),直接證明了膜蛋白STX18的跨膜結(jié)構(gòu)域通過(guò)兩次跨膜錨定于脂滴表面。
由于在體內(nèi)難以實(shí)現(xiàn)針對(duì)膜融合過(guò)程的實(shí)時(shí)監(jiān)測(cè),尤其是脂滴這一動(dòng)態(tài)變化極其頻繁的細(xì)胞器,研究團(tuán)隊(duì)嘗試在體外生化重建脂滴融合這一生物學(xué)過(guò)程。研究團(tuán)隊(duì)首先建立了基于FRET(熒光能量共振轉(zhuǎn)移)的人工脂滴Lipid mixing assay,證明了STX18-SNAP23-SEC22B的截短體和全長(zhǎng)復(fù)合物可介導(dǎo)人工脂滴Lipid mixing。由于體外脂滴Lipid mixing assay中標(biāo)記的是脂滴的磷脂單分子層,Lipid mixing assay不足以完全表征融合的發(fā)生。接著,研究團(tuán)隊(duì)首次合成了Cy3-DAG和Cy5-DAG來(lái)標(biāo)記脂滴的內(nèi)部,建立了基于FRET的人工脂滴Content mixing assay,并結(jié)合DLS(動(dòng)態(tài)光散射技術(shù))和Cyro-EM(冷凍電鏡),直接證明了STX18-SNAP23-SEC22B介導(dǎo)了脂滴融合的發(fā)生。進(jìn)一步地,研究團(tuán)隊(duì)發(fā)現(xiàn)已被報(bào)道過(guò)的脂滴融合相關(guān)蛋白CIDEC/FSP27與SNAREs之間存在互作和共定位,并且全長(zhǎng)的CIDEC/FSP27在體外可促進(jìn)SNARE介導(dǎo)的脂滴融合的發(fā)生,結(jié)合DLS assay,研究團(tuán)隊(duì)猜測(cè)CIDEC/FSP27在體外作為T(mén)ether橋連了相鄰的脂滴,促進(jìn)SNARE介導(dǎo)的脂滴融合。
那么,SNARE缺失影響脂滴融合的生理意義是什么呢?研究團(tuán)隊(duì)通過(guò)AAV敲低小鼠肝臟內(nèi)STX18,發(fā)現(xiàn)STX18的敲低可以緩解高脂飲食誘導(dǎo)的小鼠肝臟脂質(zhì)沉積。這與之前報(bào)道的敲低脂滴融合相關(guān)蛋白FSP27或Rab8a可緩解非酒精性脂肪性肝病類(lèi)似。因此,研究團(tuán)隊(duì)的發(fā)現(xiàn)進(jìn)一步提示了脂滴融合的穩(wěn)態(tài)對(duì)于脂質(zhì)有效儲(chǔ)存的重要性。
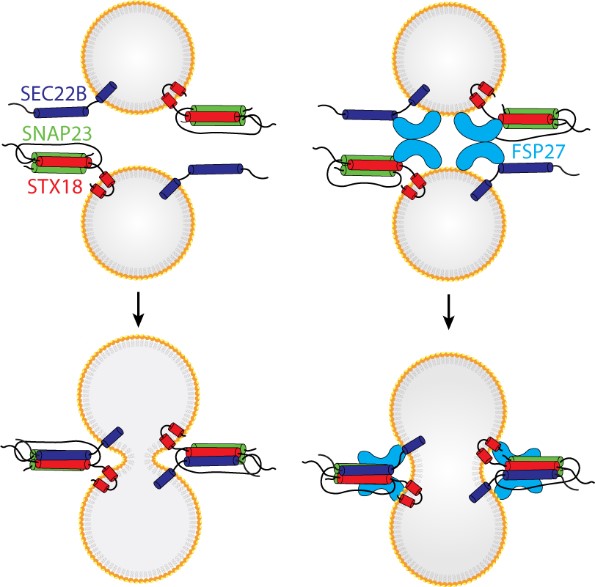
圖注:Qa SNARE STX18、Qbc SNARE SNAP23和R SNARE SEC22B形成SNARE復(fù)合物,使相鄰的脂滴膜結(jié)構(gòu)受擠壓發(fā)生形變,導(dǎo)致磷脂分子的重新排列,驅(qū)動(dòng)脂滴融合。CIDEC/FSP27可通過(guò)介導(dǎo)脂滴聚集以及與SNAREs相互作用促進(jìn)SNAREs介導(dǎo)的脂滴融合。
鐘清課題組的傅宇輝博士,丁彬彬教授,留筱廈副研究員為本文共同第一作者,鐘清研究員,丁彬彬教授,留筱廈副研究員為本文的共同通訊作者。

