
近日,上海交通大學(xué)基礎(chǔ)醫(yī)學(xué)院藥理學(xué)與化學(xué)生物學(xué)系高小玲教授聯(lián)合上海中醫(yī)藥大學(xué)陳紅專教授和加拿大多倫多大學(xué)鄭崗教授在國際權(quán)威雜志《自然.納米技術(shù)》(Nature Nanotechnology)正式發(fā)表了題為“Intracerebral fate of organic and inorganic nanoparticles is dependent on microglial extracellular vesicle function”的研究論文。《自然.納米技術(shù)》同期配發(fā)《Intracerebral fate of engineered nanoparticles》新聞和評述。
納米遞藥技術(shù)的快速發(fā)展為疾病診療帶來了革命性進展,但對腦部疾病的診療仍面臨巨大挑戰(zhàn)。既往研究多聚焦于各種納米遞藥系統(tǒng)跨血腦屏障藥物遞送效率和效應(yīng),而對于入腦后納米遞藥系統(tǒng)的腦內(nèi)轉(zhuǎn)運和清除模式(腦內(nèi)命運)等缺乏了解,極大限制了納米遞藥系統(tǒng)的有效安全應(yīng)用的拓展。一方面,納米遞藥系統(tǒng)為藥物的高效腦內(nèi)靶向遞送并診治疾病提供更多機會;另一方面,納米遞藥系統(tǒng)本身在腦內(nèi)的過量蓄積亦可能引起不可逆轉(zhuǎn)的中樞神經(jīng)系統(tǒng)(CNS)潛在毒副作用。因此,深入探討納米遞藥系統(tǒng)入腦后的命運決定機制及其調(diào)控方案將為其安全應(yīng)用提供重要依據(jù)和保障,具有重要的理論價值和現(xiàn)實意義。
高小玲課題組長期聚焦CNS的藥物遞送研究,特別關(guān)注遞藥技術(shù)的高效性和安全性,在國際上率先開展了納米遞藥系統(tǒng)的腦內(nèi)命運和清除機制研究。該研究發(fā)現(xiàn)有機材料構(gòu)成的重組高密度脂蛋白和聚乙二醇-聚乳酸納米粒可經(jīng)過膠質(zhì)淋巴系統(tǒng)途徑向腦外快速清除;而金納米粒、量子點、氧化鐵納米顆粒等無機納米粒的腦清除過程緩慢,存在腦內(nèi)蓄積和引發(fā)神經(jīng)毒性的風(fēng)險。小膠質(zhì)細胞是CNS常駐巨噬細胞,在清除異物,維持腦內(nèi)穩(wěn)態(tài)發(fā)揮重要作用。小膠質(zhì)細胞攝取有機納米粒后,將其轉(zhuǎn)運至血管旁,使其通過膠質(zhì)淋巴系統(tǒng)向腦外清除;而無機納米粒被小膠質(zhì)細胞捕獲后,長時間滯留于胞內(nèi),無法外排。
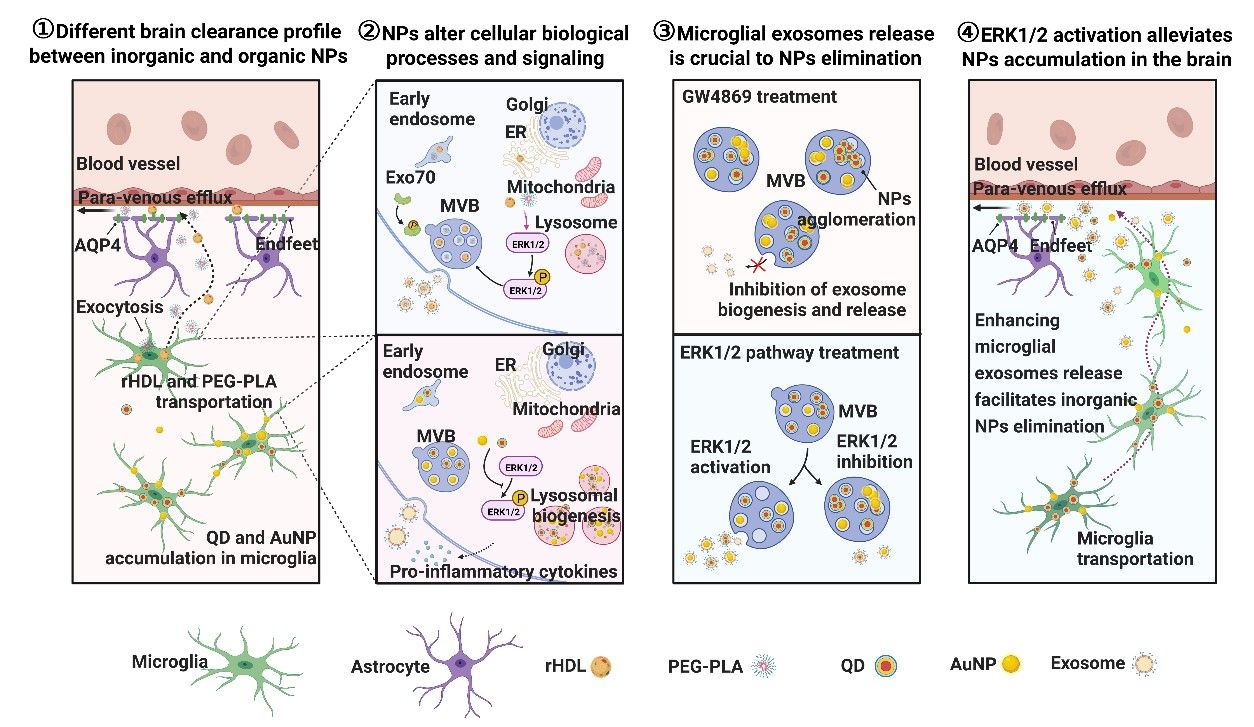
為了揭示小膠質(zhì)細胞介導(dǎo)不同材料納米粒腦內(nèi)轉(zhuǎn)運和清除差異的機制,研究人員分析比較了小膠質(zhì)細胞內(nèi)各納米粒的分布、轉(zhuǎn)運與外排方式,并采用轉(zhuǎn)錄組學(xué)等系統(tǒng)生物學(xué)方法比較各種納米粒對細胞生物學(xué)過程和關(guān)鍵信號通路的影響。發(fā)現(xiàn)有機、無機種類納米粒處理后,小膠質(zhì)細胞內(nèi)與胞內(nèi)囊泡轉(zhuǎn)運、細胞外囊泡(EVs)發(fā)生和釋放等過程密切相關(guān)的細胞外信號調(diào)節(jié)激酶(ERK1/2)信號通路發(fā)生了不同方向的變化:無機納米粒處理抑制小膠質(zhì)細胞的ERK1/2通路,EVs分泌減少;而有機納米粒促進小膠質(zhì)細胞ERK1/2通路激活,胞內(nèi)囊泡轉(zhuǎn)運增加,EVs分泌增加。而抑制EVs分泌,顯著減少納米粒從小膠質(zhì)細胞外排,抑制其腦內(nèi)轉(zhuǎn)運和清除。以上結(jié)果表明,小膠質(zhì)細胞的EVs分泌可能是其介導(dǎo)納米粒腦內(nèi)轉(zhuǎn)運和清除的關(guān)鍵機制,相關(guān)途徑受ERK1/2信號通路調(diào)控。
為實現(xiàn)納米遞藥系統(tǒng)的腦內(nèi)命運調(diào)控,研究人員進一步提出通過藥理學(xué)手段激活ERK1/2通路,促進小膠質(zhì)細胞以EVs分泌方式促進納米粒從腦實質(zhì)轉(zhuǎn)運至血管旁清除,從而減少腦內(nèi)納米粒的腦內(nèi)蓄積。研究發(fā)現(xiàn)ERK1/2激動劑帕莫酸處理后,小膠質(zhì)細胞分泌的EVs數(shù)量顯著增多,且在EVs伴隨包裹大量QD和AuNP。重要的是,在帕莫酸共注射情況下,量子點和金納米粒的腦清除速率分別提高至原來的5.48倍和28.56倍。小膠質(zhì)細胞耗竭和膠質(zhì)淋巴系統(tǒng)抑制實驗證實帕莫酸促進的無機納米粒腦清除同樣是通過小膠質(zhì)細胞介導(dǎo)的膠質(zhì)淋巴系統(tǒng)途徑實現(xiàn)的。
綜上所述,該研究通過闡明不同納米遞藥系統(tǒng)腦清除差異的原因,揭示小膠質(zhì)細胞EVs對于腦內(nèi)納米粒的清除至關(guān)重要;發(fā)現(xiàn)通過激活ERK1/2通路,可促進小膠質(zhì)細胞EVs的釋放,有效減輕納米粒特別是具有神經(jīng)毒性的無機納米粒的腦內(nèi)蓄積。以上發(fā)現(xiàn)填補了納米遞藥系統(tǒng)的腦內(nèi)命運調(diào)控領(lǐng)域研究的空白,同時為納米遞藥系統(tǒng)的腦內(nèi)安全應(yīng)用提供了重要的理論和實驗基礎(chǔ)。
上海交通大學(xué)醫(yī)學(xué)院高金超博士為該論文的第一作者,高小玲教授、上海中醫(yī)藥大學(xué)陳紅專教授和加拿大多倫多大學(xué)鄭崗教授為共同通訊作者。該工作得到了國家自然科學(xué)基金、國家重點研發(fā)計劃、上海市科委、上海市科委項目的資助。上海交通大學(xué)醫(yī)學(xué)院基礎(chǔ)醫(yī)學(xué)公共技術(shù)平臺和上海交通大學(xué)分析測試中心提供了重要的設(shè)備和技術(shù)支持。

