2月18日,醫(yī)學(xué)院實驗動物科學(xué)部陳學(xué)進研究員課題組和附屬瑞金醫(yī)院內(nèi)分泌代謝病研究所李小英教授課題組的合作研究成果在國際一流學(xué)術(shù)雜志Cell子刊
- Cell Metabolism (影響因子:17.565)上在線發(fā)表。研究論文題為“Paternal Psychological
Stress Reprograms Hepatic Gluconeogenesis in
Offspring”。該項工作全部由醫(yī)學(xué)院科研人員在國內(nèi)獨立完成,陳學(xué)進研究員的博士研究生吳鈴為論文的第一作者,瑞金醫(yī)院內(nèi)分泌代謝病研究所的陸炎博士和焦陽博士為論文的共同第一作者。研究首次發(fā)現(xiàn),父親的心理應(yīng)激,通過表觀遺傳等機制調(diào)控子代的糖代謝狀況,進一步證實了環(huán)境因素介導(dǎo)的跨代遺傳調(diào)控作用。
當(dāng)今社會,隨著經(jīng)濟水平的發(fā)展,生活方式的轉(zhuǎn)型,焦慮、緊張、抑郁等心理壓力與應(yīng)激日益頻繁,已嚴重危害人類健康。大量人群流行病學(xué)研究表明,心理應(yīng)激(Psychological
stress)與多個疾病的發(fā)生發(fā)展密切相關(guān),如神經(jīng)退行性疾病、心血管疾病、腫瘤、2型糖尿病等。此外,近年來的研究表明,母親的心理應(yīng)激,尤其是妊娠期間的應(yīng)激,可促進子代肥胖和2型糖尿病的發(fā)生。但父親應(yīng)激,能否影響或調(diào)控子代的糖代謝情況,目前尚無文獻報道。鑒于此,雙方課題組通力協(xié)作,以C57BL/6小鼠為動物模型,系統(tǒng)的探討了這一跨代遺傳現(xiàn)象及背后的分子機制。研究人員將8周齡雄性小鼠置于50毫升離心管中(Restraint
stress),每天2小時,持續(xù)2周 (Stress組)。對照組小鼠
(Control組)在此期間,自由進食與活動。2周后,將兩組小鼠分別與正常雌鼠交配,進而獲得子代小鼠
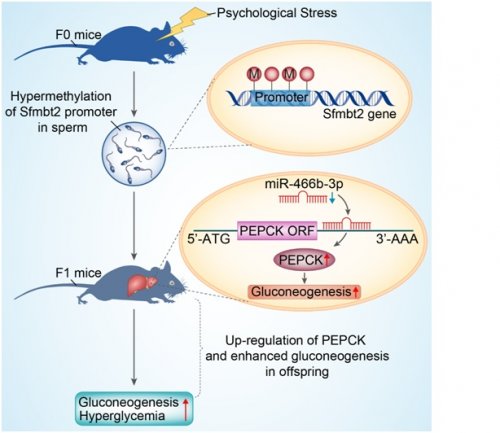
(F1)。進而,課題組詳細觀察了兩組小鼠(Control-F1、Stress-F1)的糖代謝表型,并發(fā)現(xiàn):Stress-F1小鼠表現(xiàn)為血糖升高,丙酮酸耐量實驗表明肝臟糖異生和肝糖輸出能力增強,而葡萄糖和胰島素耐量實驗表明胰島素敏感性并未改變。在基因表達層面,Stress-F1小鼠肝臟PEPCK的蛋白水平顯著增加,但mRNA無明顯改變,提示PEPCK的表達可能受到轉(zhuǎn)錄后水平的調(diào)節(jié)。由此,課題組通過MicroRNA表達譜芯片,篩選出調(diào)節(jié)PEPCK表達的一個MicroRNA:
miRNA-466b-3p的表達在Stress-F1小鼠肝臟中顯著下調(diào)。在此基礎(chǔ)上,課題組發(fā)現(xiàn)父親應(yīng)激后,血清糖皮質(zhì)激素水平顯著升高,引起精子miRNA-466b-3p啟動子區(qū)域甲基化程度的增加,并遺傳至子代小鼠,導(dǎo)致其肝臟中miR-466b-3p的表達下調(diào),引起PEPCK蛋白表達的增加,從而引發(fā)子代小鼠糖異生增加,血糖升高。
本研究首次發(fā)現(xiàn),父親的心理應(yīng)激,通過表觀遺傳等機制,調(diào)控子代的糖代謝狀況。有趣的是,近年來,父親至子代的跨代遺傳調(diào)控作用(Intergeneration),已在多個動物模型上被發(fā)現(xiàn)。例如,給予父親高脂、低蛋白等飲食處理后,可影響子代胰島、肝臟中糖脂代謝相關(guān)基因的表達,進而影響子代小鼠的糖脂代謝穩(wěn)態(tài)。因此,本研究進一步證實了環(huán)境因素介導(dǎo)的跨代遺傳調(diào)控作用。而這些結(jié)果,將為日后人群層面相關(guān)疾病的研究提供有益的線索和理論基礎(chǔ)。
陳學(xué)進研究員課題組長期致力于生殖、胚胎發(fā)育研究,李小英教授課題組則擅長于糖脂代謝的病理生理機制研究。在本項研究中,雙方取長補短,精心合作,從而在該領(lǐng)域取得了這一重要研究進展。該項工作也得到國家科技部973重點研究計劃和國家自然科學(xué)基金項目的資助。
文章鏈接:http://www.cell.com/cell-metabolism/fulltext/S1550-4131(16)30006-7

