11月1日,國(guó)際著名學(xué)術(shù)期刊《The Journal of Clinical
Investigation》在線發(fā)表了上海交通大學(xué)醫(yī)學(xué)院細(xì)胞凋亡與分化教育部重點(diǎn)實(shí)驗(yàn)室鄭俊克課題組完成的題為“Sorting
protein VPS33B regulates exosomal autocrine signaling to mediate
hematopoiesis and
leukemogenesis”的最新研究成果。論文首次報(bào)道了干性相關(guān)的分泌性蛋白以外泌體形式通過(guò)自分泌作用調(diào)控造血干細(xì)胞和白血病干細(xì)胞的自我更新能力。
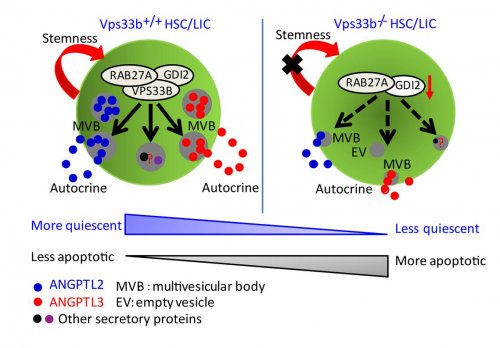
關(guān)于干細(xì)胞自我更新調(diào)控的研究,一直是干細(xì)胞領(lǐng)域研究的重點(diǎn)。已知一系列分泌性蛋白對(duì)造血干細(xì)胞的自我更新具有重要的調(diào)控作用,但這些蛋白產(chǎn)生、成熟和釋放的機(jī)制亟待闡明。鄭俊克課題組揭示了一些干性相關(guān)分泌蛋白(如ANGPTL2,
ANGPTL3和TPO等)的新型分泌方式-外泌體分泌途徑,并且鑒定了一個(gè)關(guān)鍵基因VPS33B在此過(guò)程的重要調(diào)控作用。VPS33B缺失可導(dǎo)致造血干細(xì)胞和白血病干細(xì)胞外泌體成熟和釋放受損以及自我更新能力的急劇丟失,而這一過(guò)程在一定程度上可被體外過(guò)表達(dá)或血漿中的ANGPTL2或ANGPTL3外泌體所修復(fù)。在機(jī)制方面,他們發(fā)現(xiàn)了一個(gè)新的VPS33B/GDI2/RAB11A/RAB27A通路調(diào)控分泌蛋白的外泌體釋放過(guò)程。該項(xiàng)研究勾勒出了一個(gè)全新的造血干細(xì)胞和白血病干細(xì)胞的外泌體調(diào)控網(wǎng)絡(luò),對(duì)于了解其他類型干細(xì)胞的囊泡運(yùn)輸及外泌體分泌調(diào)控機(jī)制具有重要意義,也為腫瘤治療提供了新方向。
該工作由基礎(chǔ)醫(yī)學(xué)院的鄭俊克課題組和另外兩位共同通訊作者陳國(guó)強(qiáng)和劉俊嶺所在課題組共同合作完成,第一作者谷浩也是陳國(guó)強(qiáng)教授在中科院健康所招收的博士研究生。該項(xiàng)工作得到了中組部千人計(jì)劃、基金委優(yōu)青、杰青、科技部973等項(xiàng)目的大力資助。
文章鏈接https://www.jci.org/articles/view/87105

